이번 포스트에서는 수소결합(hydrogen bond)의 중요성에 대해 알아보자.

일단 hydrogen bond는 위와 같이 다양한 biological한 반응, 혹은 구조형성에 밀접하게 관련되어 있음.

위 그림은 cellulose의 구조를 나타내주고 있는데, 보면 한 사슬 안에서도 hydrogen bond가 이루어져 있고(intramolecular hydrogen bond), 두 사슬 간에서도 hydrogen bond가 이루어져 있음(intermolecular hydrogen bond)을 알 수 있음. 결과적으로 cellulose의 구조 형성에 hydrogen bond가 중요하게 작용함.

한편 위 그림과 같이 enzyme과 substrate간의 상호작용(혹은 binding)에서도 hydrogen bond가 중요하게 사용될 수 있음. (위 그림에서는 특히 ribonuclease와 그의 substrate인 Uracil간의 상호작용이 나타나 있음)
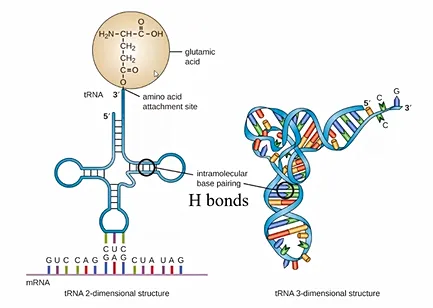
또 위 그림에 나타난 것과 같이 위 그림에 나타난 것과 같이 tRNA가 3차원 구조를 형성하는 과정에서도 RNA 내부의 base들 간의 hydrogen bond가 매우 중요함.
그 밖에 hydrogen bond는 water의 특수한 property가 만들어지는 이유임. 대표적인 예로, 물이 얼어서 생기는 ice가 물보다 밀도가 도리어 낮아져서 물에 둥둥 뜨는 현상을 들 수 있음.

보면 위 그림과 같이 온도가 낮아질 시 water 분자들이 서로 규칙화되면서 hexagonal한 구조를 이루게 됨. (이 과정에서 질서정연해지면서 entropy가 낮아짐) 한편 이 경우에는 한 분자의 물이 최대 수소결합의 수인 4개에 거의 육박할 정도로 maximal하게 hydrogen bond를 형성하고 있음. (위 오른쪽 그림에서 3D를 상상해보면 수긍이 갈 것임) 한편 위 그림 왼쪽과 같이 온도가 높아져 water가 되면 이 때는 물분자들이 random하게 배열하게 되고, 그 결과 물 분자 하나가 4개보다 훨씬 작은(3.3개 이하) 수의 hydrogen bond를 형성하게 됨.
그런데 이런 식으로 ice가 규칙적으로 배열되는 과정에서, hexagonal structure가 형성되므로 위 그림에서도 알 수 있듯 water일 때보다 도리어 density는 더 감소하게 됨. 이 때문에 물에 ice가 뜨는 것임.
한편 water는 좋은 solvent(용매)이기도 함. 특히나 water는 amino acid, peptide, small alcohol, carbohydrate와 같은 charged molecule, 혹은 polar molecule들에 대해 특히 더 좋은 solvent임. 반면 nonpolar gases, aromatic molecules, aliphatic chain molecule등의 nonpolar molecule들에 대해서는 굉장히 나쁜 solvent임.

위 그림에 물에 잘 녹는 polar molecule들과 물에 잘 녹지않는 nonpolar molecule들의 예시가 나타나 있으므로 참고할 것. 참고로 이 때 Amphipathic이란 분자 내에 polar한 성질과 nonpolar한 성질이 모두 공존하고 있는 것을 말함.
다음 포스트에서는 비공유결합성 상호작용(noncovalent interaction)들과 관련된 내용들에 대해 살펴보자.
'전공자를 위한 생물학 > 생화학' 카테고리의 다른 글
| [생화학] 1.5 : 물의 이온화(ionization) - 1 (0) | 2024.11.03 |
|---|---|
| [생화학] 1.4 : 삼투압(osmotic pressure) (0) | 2024.11.03 |
| [생화학] 1.3 : 비공유결합성 상호작용(noncovalent interaction) - 2 (0) | 2024.11.03 |
| [생화학] 1.3 : 비공유결합성 상호작용(noncovalent interaction) - 1 (0) | 2024.11.03 |
| [생화학] 1.1 : 물의 특징 (0) | 2024.11.02 |