이번 포스트부터는 뉴클레오타이드의 생합성 과정에 대해 알아보자.

nucleotide의 구조는 위 그림과 같음. 보면 ribose, 혹은 deoxyribose에 phosphate가 붙어있고, 1번 탄소에 purine base, 혹은 pyrimidine base가 연결되어 있는 구조임. 이 때 purine base에는 adenine, guanine이 포함되고, pyrimidine base에는 cytosine, uracil, thymine이 포함되어 있음.
nucleotide의 biosynthesis는 de novo pathway에 의해서도, salvage pathway에 의해서도 일어날 수 있음. de novo pathway는 amino acid, ribose 5-phosphate, CO2, NH3와 같은 metabolic precursor로부터 nucleotide를 합성하는 과정을 말하며, salvage pathway는 nucleotide breakdown 과정에서 release된 free base, nucleoside 등을 재활용해서 nucleotide를 합성하는 과정을 의미함.
참고로 malaria를 포함한 많은 parasite들은 de novo biosynthesis pathway를 통해 nucleotide를 합성하지 못하므로 host의 free base, nucleoside에 totally dependent하게 nucleotide를 합성함. (totally depends on salvage pathway) 따라서 salvage pathway를 inhibition할 수 있는 compound는 antiparasite drug로 사용될 수도 있음.
de novo biosynthesis of Purine nucleotides
우선 purine nucleotide의 de novo biosynthesis 과정에 대해 살펴보자. 흥미롭게도 purine nucleotide의 base는 ribose에 붙어있는 채로 합성됨.

위 그림에는 purine base를 구성하는 각 원소들이 어디로부터 유래되었는지가 표시되어 있음.
purine 합성의 결과 AMP, GMP의 형태의 화합물이 가장 먼저 만들어지게 됨. (pyrimidine 합성시에는 이와 다른 양상이 관찰됨)

합성 시 시작물질은 위 그림상에 나타나 있는 PRPP(5-phosphoribosyl 1-pyrophosphate)임. 여기에 purine에 해당하는 base가 serial한 reaction을 거쳐 합성되는 것임.
이제 본격적인 합성과정을 살펴보자.

(참고로 위 그림상에서 R로 표시된 부분이 PRPP backbone임) 위 그림에 나타나 있는 것처럼 우선 PRPP에 glutamine으로부터 유래된 amino group이 첨가되어서 5-phospho-β-D-ribosylamine이 만들어짐. (이어서 이곳에 glycine이 들어가고, amino gorup의 N과 일종의 peptide bond를 형성하면서 연결되어서 GAR이 형성됨. 이후 folate에 carrying되어온 formyl C가 첨가되어서 FGAR이 됨.

이후 FGAR은 glutamine으로부터 amino group을 하나 더 전달받아서 FGAM이 됨. 이어서 FGAM은 ATP를 소모하는 반응의 결과 AIR의 imidazole ring 형태로 변형됨.

참고로 이 때 FGAM이 AIR로 변환되는 반응은 위 그림에 나타나 있는 imine의 형성 반응에 해당함.
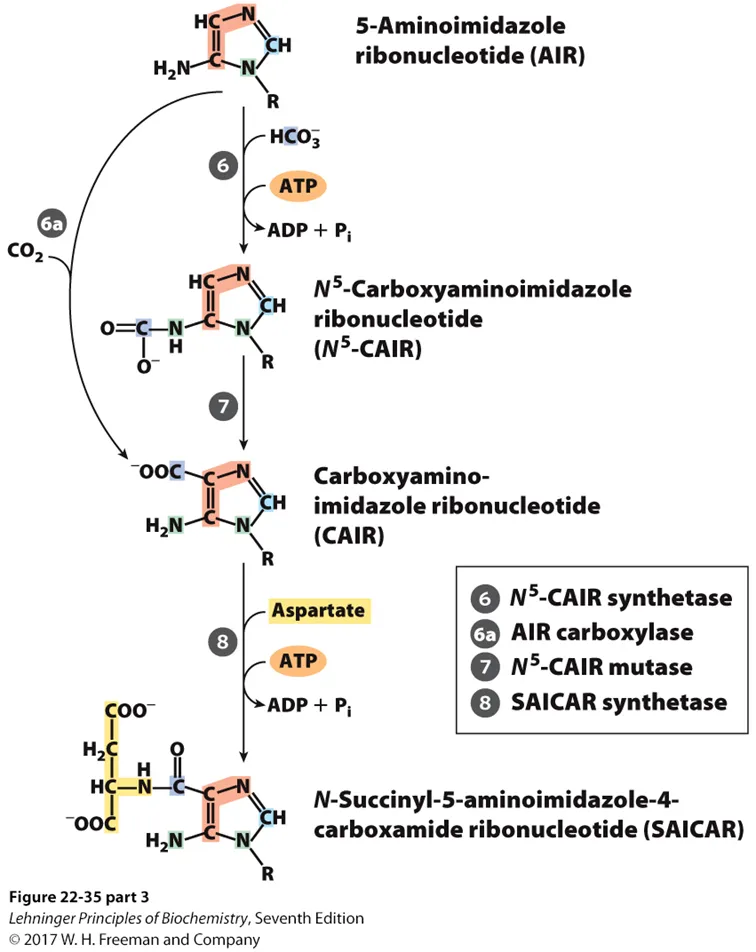
이어서 위와 같은 반응이 일어남. 보면 AIR에 HCO3-로부터 유래한 C가 하나 더 첨가되고(이 과정에서 ATP가 한 분자 소모됨) 그 결과 N5-CAIR이 만들어짐. 이후 N5-CAIR 내부의 carboxyl group의 위치가 mutase에 의해 바뀌어서 CAIR이 형성됨. 다만 사실 higher eukaryote에서는 이런 2 step의 반응 대신에, AIR에서 CO2가 첨가되는 하나의 반응을 통해서 곧바로 CAIR이 형성될 수 있음. 이어서 ATP의 분해와 coupling된 채 CAIR에 aspartate가 첨가되는 반응이 일어나게 되면 결과적으로 SAICAR라는 화합물이 만들어짐.

이후 SAICAR에서 fumarate가 떨어져나가며 aspartate로부터 유래한 N 하나만 남은 AICAR가 형성됨. 이어서 folate에 carrying되어온 formyl C가 하나 추가적으로 첨가되고(구체적으로는 amino group에 첨가됨) 그 결과 FAICAR가 형성됨. 이후 마지막으로 물이 빠져나가며 imine이 만들어지며 ring이 close됨. 이런 과정을 거쳐 최종적으로 만들어지는 화합물이 바로 inosinate(IMP)임.
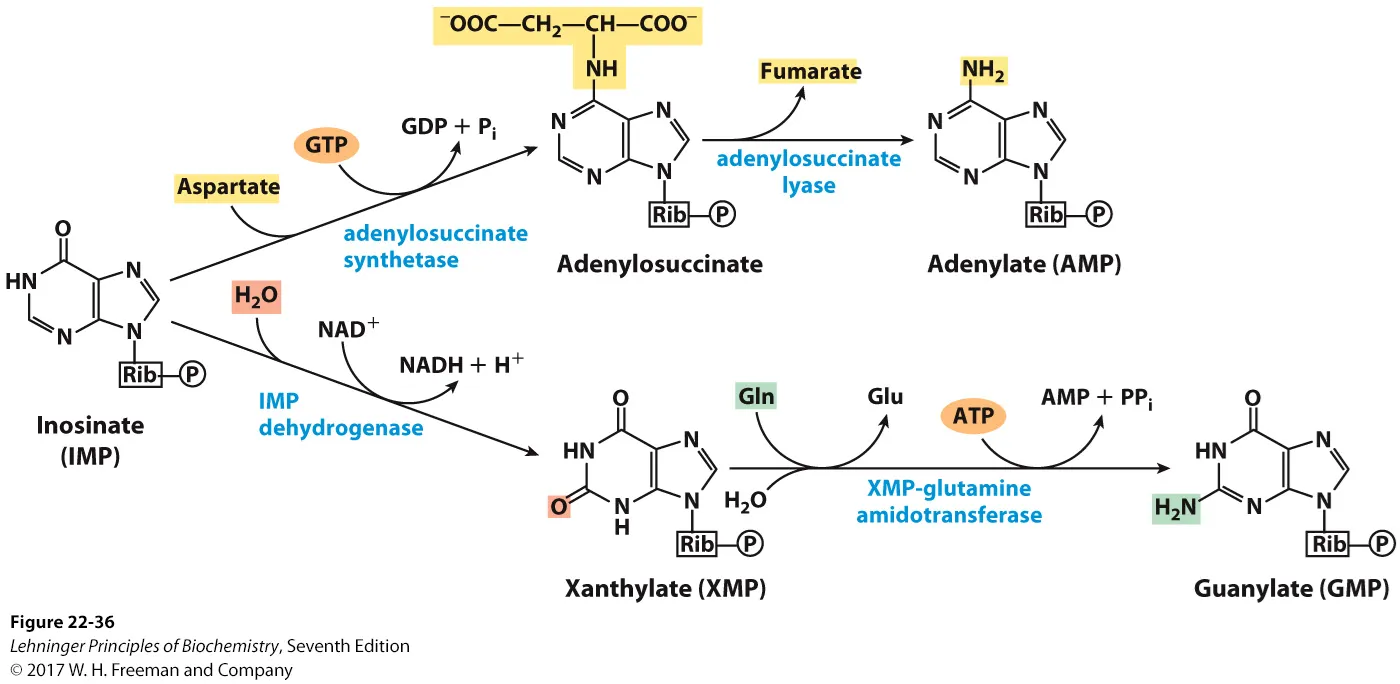
한편 IMP로부터 위와 같은 과정에 의해 AMP, GMP가 만들어질 수 있음. 우선 IMP로부터 AMP가 만들어지는 과정을 살펴보자. 보면 GTP의 가수분해와 coupling되어 IMP에 aspartate가 첨가됨. 이어서 fumarate가 떨어져나가며 adenylate(AMP)가 만들어짐. 다음으로 IMP로부터 GMP가 만들어지는 과정을 살펴보자.
보면 우선 물이 첨가되며 IMP가 XMP로 oxidation되고, 이어서 ATP의 가수분해와 coupling되어서 glutamine으로부터 유래된 amino group이 첨가됨. 그 결과 guanylate(GMP)가 만들어짐. 참고로 이 때 AMP 합성 과정에서의 rate limiting step을 촉매하는 효소는 adenylosuccinate synthetase이고, GMP 합성 과정에서의 rate limiting step을 촉매하는 효소는 XMP-glutamine amidotransferase임.
다음으로 purine biosynthesis와 관련된 regulation 기작에 대해 살펴보자.

regulation과 관련된 모식도가 위 그림상에 나타나 있음. 보면 우선 IMP, GMP, AMP가 PRPP→5-phosphoribosylamine으로 변환되는 반응에 대한 allosteric inhibitor로 작동하게 됨. 그 밖에, AMP는 IMP로부터 AMP가 만들어지는 반응을 억제하고, GMP는 IMP로부터 GMP가 만들어지는 반응을 억제함. 사실 이런 억제가 가능한 데에는 중요한 이유가 있는데, 바로 AMP 합성과정에서는 GTP가 energy source로 쓰이고, GMP 합성과정에서는 ATP가 energy source로 쓰인다는 것임.
그렇기에 AMP, GMP에 의해 각각의 synthesis가 효과적으로 저해될 수 있고 결국 GMP와 AMP의 합성량이 well balance된 채로 유지될 수 있는 것임. (실제로 상황을 상상해보면, AMP가 많아질 시 AMP 합성량이 감소하고, GMP가 많아질 시 GMP 합성량이 감소함. 이 결과 IMP의 누적이 일어날 수 있으며, 많아진 IMP는 PRPP가 다음 step으로 변환되는 것을 block하게 됨) 한편 그 밖에, AMP는 ATP로부터 하나의 인산기를 제공받아 ADP가 된 후 ribose 5-phosphate가 PRPP로 변환되는 반응을 억제하기도 함. 즉, AMP에 의해 overall reaction도 turn-off될 수 있는 것임.
다음 포스트에서 이어서 살펴보자.
'전공자를 위한 생물학 > 생화학' 카테고리의 다른 글
| [생화학] 21.3 : 뉴클레오타이드의 생합성 - 3 (0) | 2025.04.18 |
|---|---|
| [생화학] 21.3 : 뉴클레오타이드의 생합성 - 2 (0) | 2025.04.18 |
| [생화학] 21.2 : 아미노산 유도체의 생합성 - 3 (0) | 2025.04.11 |
| [생화학] 21.2 : 아미노산 유도체의 생합성 - 2 (0) | 2025.04.11 |
| [생화학] 21.2 : 아미노산 유도체의 생합성 - 1 (0) | 2025.04.11 |