이번 포스트에서는 hemoglobin의 산소 affinity가 pH에 따라 어떻게 달라지는지에 대해 알아보자.
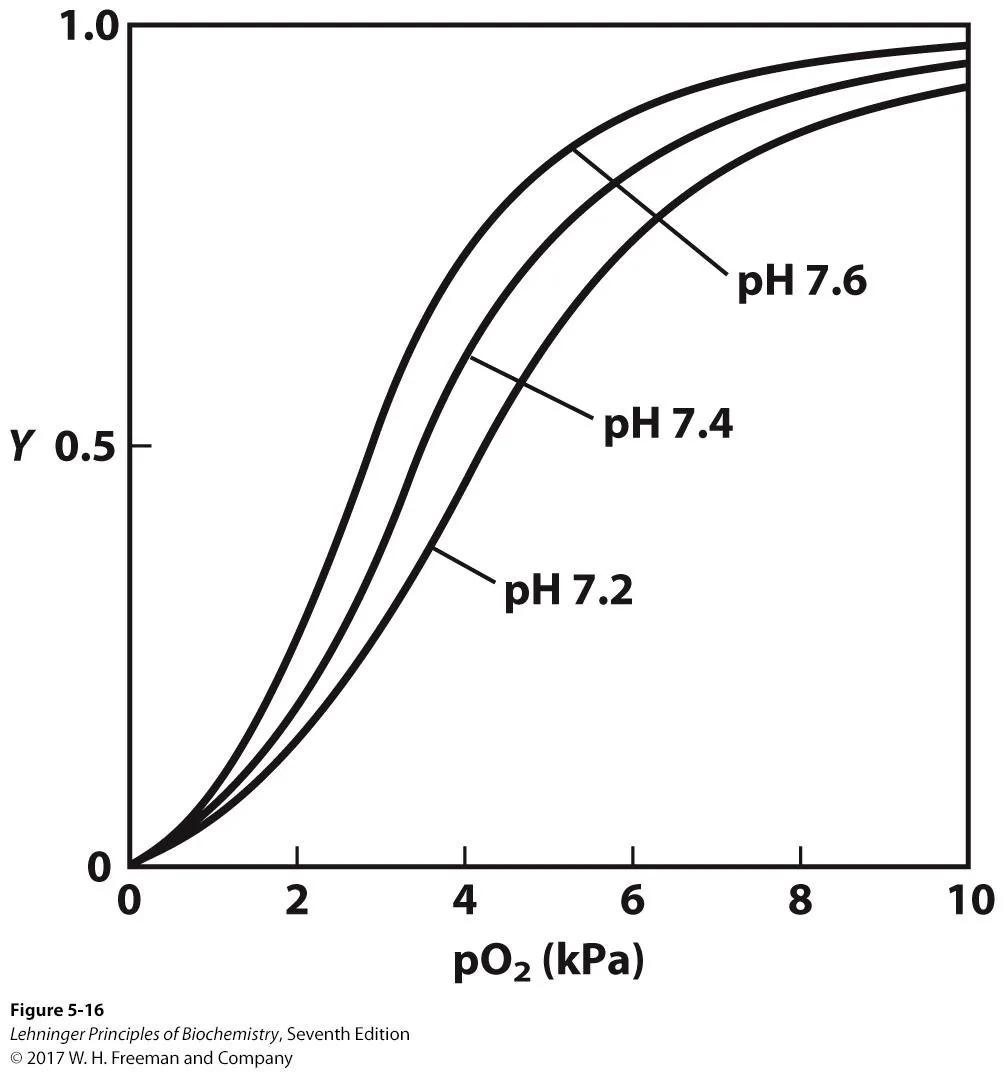
위 graph에서 Y가 0.5일 때의 부분압을 보면 Kd값을 알 수 있음. 보면 결과적으로 pH가 낮을수록 Kd값이 커짐. 이 말인즉슥 pH가 낮을수록 hemoglobin의 O2 affinity가 떨어짐.

우리 몸에 존재하는 gas 형태의 CO2는 물에 잘 녹지 않으므로 bubble을 형성할 수 있어서 위험함. 따라서 위와 같은 반응에 의해서 물에 더 잘 녹은 bicarbonate인 HCO3-가 만들어지게 됨. 그런데 이 과정에서 수소이온도 많이 증가함. 즉, 결과적으로 이산화탄소가 많은 지역의 pH는 (위 반응에 의해) 낮아지게 됨.
그런데 이산화탄소가 많은 곳은 active하게 metabolize하는 tissue일 것이고 이 곳에서는 O2가 다른 조직에서보다 더 많이 필요할 것임. 이 때 앞서의 효과가 아주 유용함. 즉, pH가 낮은 부분에서 hemoglobin이 산소를 더 잘 release하게되므로 actively metabolizing tissue에 산소를 더 많이 공급할 수 있게 되는 것임.
그렇다면 구체적으로 어떻게 pH가 Hb 의 산소와의 affinity를 변화시킬까. 이는 앞서 봤던 Hb의 His146에 작용하면서 가능해짐. (참고로 이 때 His는 physiological condition과 pKa가 비슷함. 따라서 이 녀석은 쉽게 + charging되었다가, 그렇지 않았다가를 왔다갔다할 수 있음) 만약 주변에 pH가 낮아지게 되면 주변부에 H+가 많아질 것이고, 그 결과 His도 protonation되기 쉬워져서 결과적으로 더 + charge를 많이 띄게 될 것임. 그 결과 앞서 봤던 T state에서의 interaction이 더 잘 일어나게 되어서 결과적으로 T state가 더 stable해짐. 이 말인즉슨 R state로의 전환이 더 잘 안되게 되어 산소 release가 더 많이 일어나게 됨.
이러한 현상을 Bohr effect(보어 효과)라 함.

한편, Hb는 이산화탄소를 tissue에서 다시 lung으로 운반해주는 역할도 함. 이 때 위와 같이 hemoglobin의 N terminal 부분과 CO2가 결합하게 됨. 이 과정에서 만들어지는 carbamino-terminal residue는 - charge를 띄고 있고, 그 결과 주변의 + charge residue와 salt-bridge interaction을 하게 되어서 결과적으로 T state를 더 안정화시켜주는 역할을 하기도 함. 게다가 추가적으로 이 반응 과정에서 H+도 나오므로 이에 의해 Bohr effect도 강화되어서 T state가 더 안정해지게 됨.

그리고 사실 위 그림에 나타나 있는 2,3-bisphosphoglycerate(2,3-BPG)도 hemoglobin과 밀접하게 관련되어 있음. 특히 이 녀석은 hemoglobin의 cooperativity가 clear하게 관찰되게끔 하는데 도움을 줌.
이 녀석은 negative heterotropic regulator임.

위 그림에서와 같이 T state에서의 가운데 빈 부분에 2,3-BPG가 결합하고 그 결과 T state가 더 안정해짐. 그 결과 산소가 더 잘 안 붙는 형태가 됨. 따라서 이 녀석이 negative heterotropic regulator인 것임. (한편 R state가 되기 더 어려워지긴 하지만, 일단 R state가 되면 b와 같은 구조가 되므로 가운데에 2,3-BPG가 붙을 수 없음)
2,3-BPG는 우리 몸 내에서 mM정도로 상당히 abundant하게 존재하고 있음.
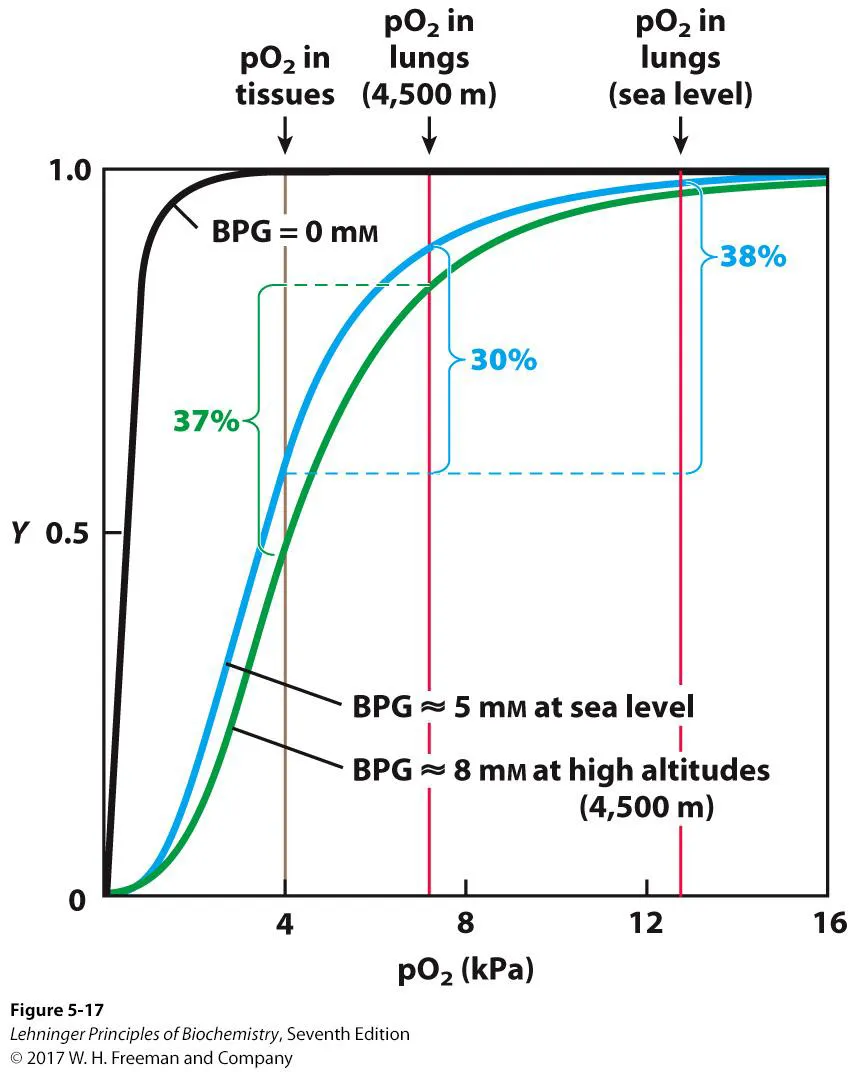
실제로 binding curve를 그려보면 BPG가 없을 때는 myoblobin과 상당히 비슷한 graph가 얻어지는 반면 BPG가 증가하면 점점 더 sigmoidal한 curve가 그려짐.
이는 사실 고산지대에서의 effective한 산소운반을 위해 상당히 중요함. 당연히 해수면 위치에 비해 고산지대에서는 산소가 부족할 것임. 이 때 일반적인 경우라면, (파란색) 고산지대로 갈 시 tissue에 전달되는 산소의 양이 거의 8%나 줄어들게 됨. 한편 고산지대에 적응한 사람들은 BPG 농도가 더 높아진 결과 초록색 graph처럼 변하게 됨. 그 결과 고산지대에서도 37% 정도의 산소를 tissue로 공급할 수 있게 됨.
한편 hemoglobin의 β chain에 있는 Glu가 Val로 바뀐다면 sickle-cell anemia가 발생할 수 있음.
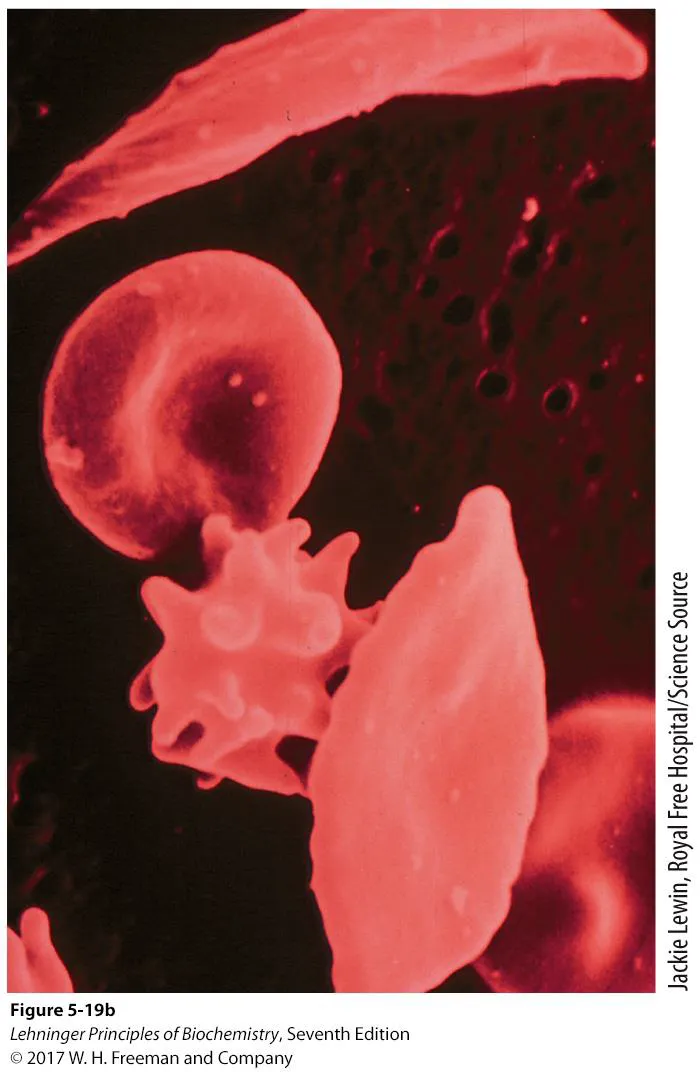
그 결과 위와 같이 낫 모양의 적혈구가 관찰되게 됨. 이들 적혈구는 굉장히 쉽게 망가지는 특징을 가지고 있음.
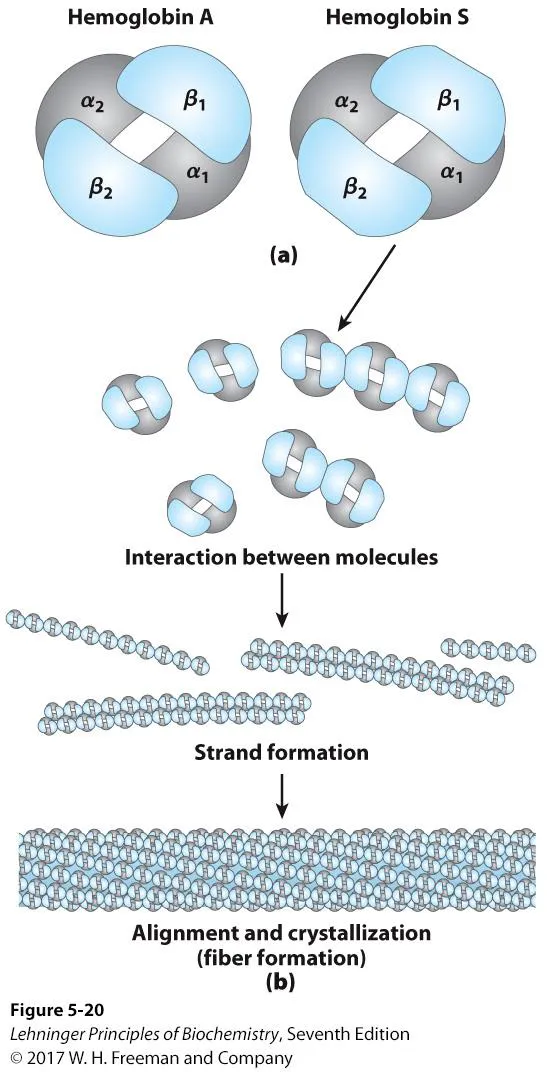
이는 위와 같이 잘못된 hemoglobin 구조 형성에 의해서 자기들끼리 aggregation되면서 amyloid-like한 구조를 형성하게 된 결과 나타나는 현상임.
homozygous mutant의 경우에는 실제로 어릴 때 다 죽게 됨. 한편 heterozygous mutant의 경우에는 한 1% 정도의 적혈구만 sickle-cell임. 이 heterozygous mutant는 아프리카에서 보다 흔하게 관찰되는데, 이는 heterozygous mutant의 경우 말라리아 resistance가 더 증가하기 때문임.
다음 포스트부터는 항원 항체반응에 대해 생화학적 관점에서 알아보자.
'전공자를 위한 생물학 > 생화학' 카테고리의 다른 글
| [생화학] 4.5 : 근육의 수축 (0) | 2024.11.07 |
|---|---|
| [생화학] 4.4 : 항원-항체 상호작용(antigen-antibody interaction) (0) | 2024.11.06 |
| [생화학] 4.3 : 헤모글로빈(hemoglobin) - 1 (0) | 2024.11.06 |
| [생화학] 4.2 : 미오글로빈(myoglobin) (0) | 2024.11.06 |
| [생화학] 4.1 : protein과 ligand (0) | 2024.11.06 |