지난 포스트에 이어 7단계부터 이어서 살펴보자.
step 7 - 1st production of ATP

다음에는 위 그림에 나타난 것과 같이 1,3-BPG와 ADP가 반응해 3-phosphoglycerate와 ATP가 만들어지는 반응이 일어나며(즉, 1,3-BPG라는 high-energy compound를 이용해 ATP를 생산하는 것), 이 반응의 효소는 phosphoglycerate kinase임. (이 효소의 이름이 kinase인 이유는, 처음에 효소의 이름을 지을 때 역반응을 생각하고 지었기 때문) 그 밖에 이 반응에는 cofactor로 Mg2+도 필요함. 한편 이 반응의 ΔG 'o는 -18.8kJ/mol인데, 애초에 1,3-BPG에서 인산기가 떨어져나가는 반응의 ΔG 'o는 대략 -49.3kJ/mol 정도 되지만 ATP의 합성에 필요한 30.5kJ/mol을 제한 정도가 전체 반응의 ΔG 'o가 된 것임.
이 반응은 꽤나 열역학적으로 favorable함. 그러나 동시에 reversible하기도 한데, 이는 상당히 작은 ΔG 'o 값을 생각하면 이상해보임. 그러나 실제로는 step 6이 reversible하므로 step 6의 역반응이 많이 일어난 결과 step 7상에서의 반응물이 적어지는 효과가 발생하므로 충분히 역반응이 일어날 수 있게 되는 것임.
step 8 - migration of the phosphate

다음 반응은 위 그림상에 나타난 것과 같이 3-phosphoglycerate에 있는 3번 위치에 달린 인산기가 2번 위치로 옮겨가 2-phosphoglycerate가 만들어지는 것으로, 이 반응에 관여하는 효소는 phosphoglycerate mutase임. 한편 이 반응에도 cofactor 형태로 Mg2+가 사용됨. 그리고 이 반응의 ΔG 'o는 거의 0에 가까운 positive여서 이 반응 또한 열역학적으로 unfavorable하고 reversible함. 다만 그럼에도 step 7에서의 효소인 phosphoglycerate kinase(PGK)에 의해서 step 8의 reactant concentration이 높게 유지되고 있어서 정반응이 잘 일어나게 됨.
이 반응의 효소로 작용하는 mutase의 경우 active site에 있는 histidine이 특히나 중요한 역할을 함. 구체적으로는 2개의 His residue가 있는데 하나는 그냥 His이고, 나머지 하나는 PTM에 의해 인산기가 달린 phosphohistidine의 형태임. (참고로 같은 분자 내에서 functional group을 transfer시키는 효소를 통틀어 mutase라 부름)
이제 이 반응의 구체적인 mechanism에 대해 알아보자.

1. 우선 위 그림에 나타나 있는 것처럼 3-phosphoglycerate가 phosphoglycerate mutase 내부에 위치하게 됨. 한편 이 때 3PG의 2번 탄소에 붙은 O가 phosphohistidine의 P를 공격하게 되고, 동시에 방금 공격에 가담한 O에 붙은 H는 나머지 하나의 His 내부에 있는 N이 뺏어가게 됨.
2. 그럴 시 2,3-BPG가 만들어지게 되는데, 이 때 1번 단계에서 phosphate이 떨어진 His의 N이 2,3-BPG 상에서 3번 탄소에 붙어있는 인산기를 공격함. 한편, 남은 O-는 주변 His에 붙어있는 수소를 공격해 OH가 됨.

3. 그럴 시 위 그림 아래와 같이 다시 enzyme 내부에는 1개의 His와 1개의 phosphohistidine이 형성되고, 2-phosphoglycerate가 생성물이 되어서 나가게 됨.
step 9 - dehydration of 2-PG to PEP

그 다음 step에서는 위 그림과 같이 2-phosphoglycerate에서 물이 빠지면서 C=C 이중결합이 생기게 되고 phosphoenolpyruvate(PEP)이 만들어지게 됨. 이런 반응은 이후 phosphate가 더 잘 떨어지게 하기 위해 매우 중요함. (실지로 2-PG 그 자체로는 phosphate donor로 작동하기에 불충분하기에 더 high-energy state의 PEP를 만들어주는 것) 한편 이 반응을 촉매하는 효소는 enolase이고, 이 반응의 ΔG 'o는 거의 0에 가까운 positive여서 이 반응 또한 열역학적으로 unfavorable하고 reversible함.
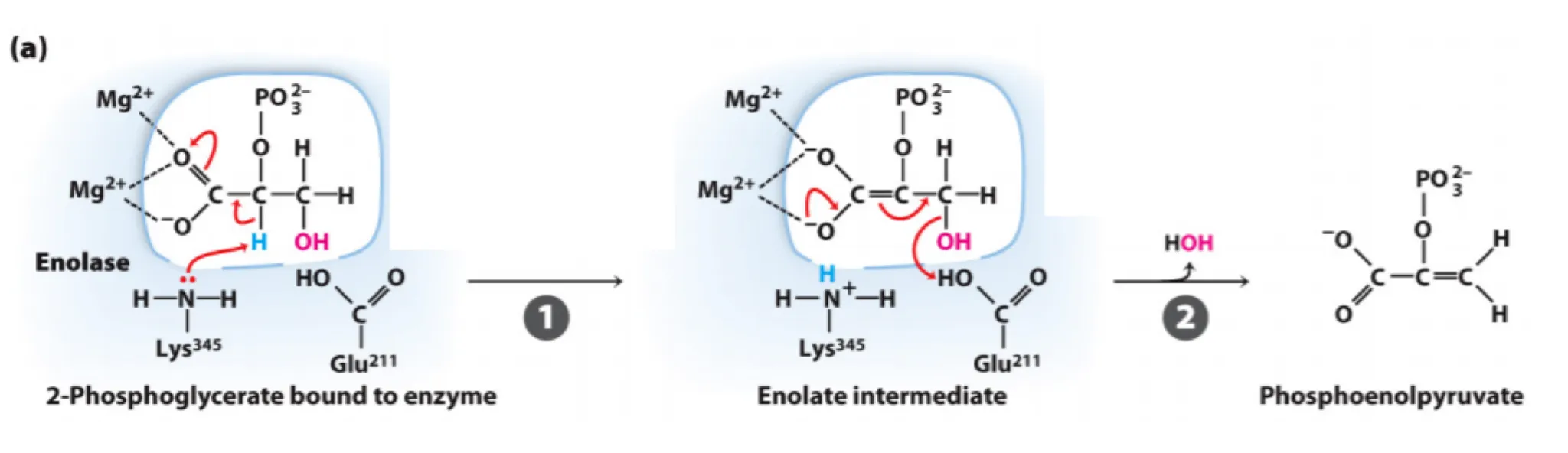
이 반응의 구체적인 mechanism은 위와 같음.
1. 우선 2-PG가 enzyme의 active site에 있는 상태에서 2-PG 끝의 carboxyl 기가 가지는 - charge를 Mg2+가 안정화시켜주고 있는 상황임.
2. 이런 상황에서 enzyme 내의 Lys이 가진 N이 2-PG의 2번탄소를 공격하게 됨. 그 결과 enolate intermediate가 형성되게 됨.
3. 이어서 enolase 내부에 있는 Glu의 OH가 공격을 받게 되고 그 결과 물이 빠져나가면서 PEP가 만들어짐.
step 10 - 2nd production of ATP
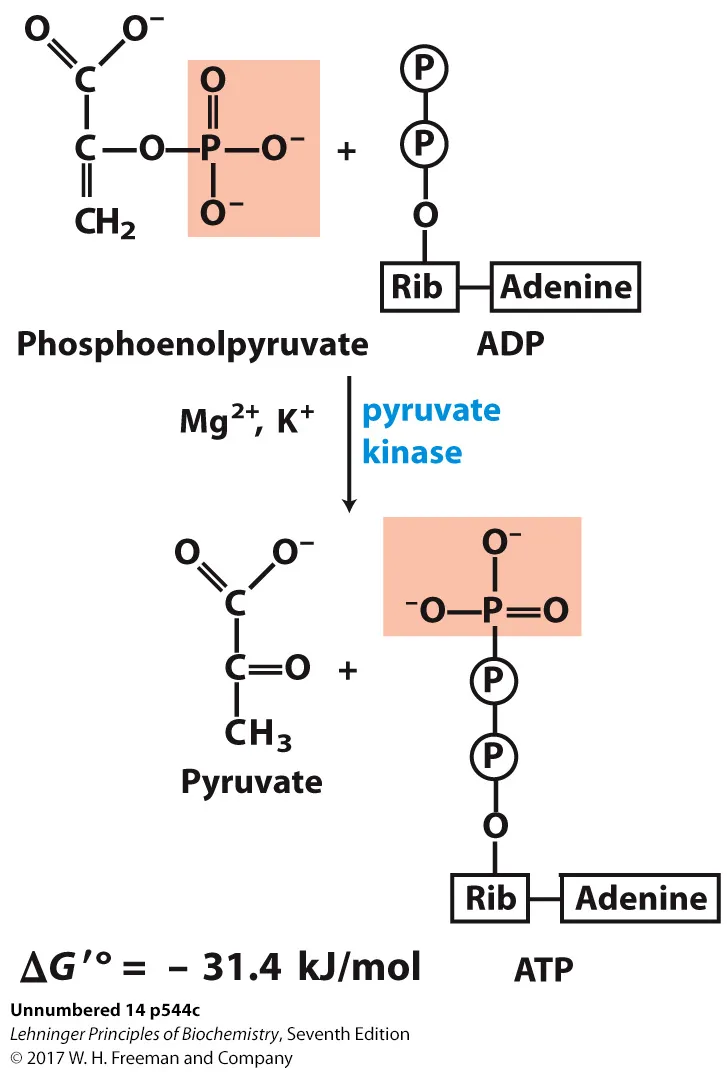
그 다음에는 위 그림에 나타나 있는 것처럼 PEP로부터 인산기가 떨어져나오면서 ADP가 ATP로 충전되고 pyruvate가 되는 반응이 일어나며, 이 반응의 cofactor로는 Mg2+, K+가, 효소로는 pyruvate kinase가 작용함. 애초에 PEP의 가수분해반응은 상당히 exergonic하기 때문에, ATP를 생산하고 남은 알짜 ΔG 'o도 상당한 음수인 것을 알 수 있음. 즉, 이 반응은 열역학적으로 favorable하고 irreversible함.
이 반응은 기본적으로 keto-enol tautomerization과 관련되어 있음.
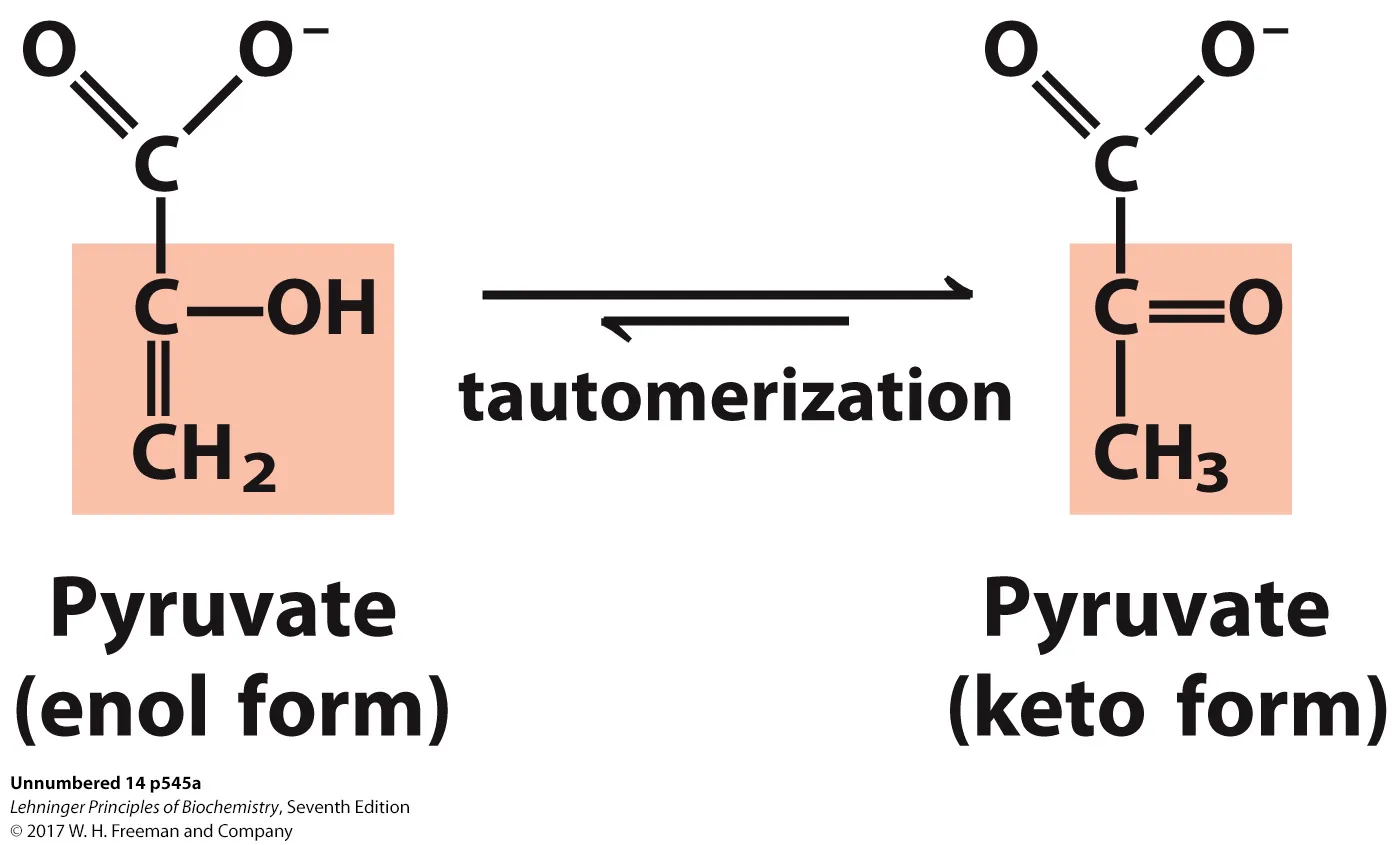
실제로 앞서의 반응에서 생성된 enol form의 pyruvate는 위 그림과 같이 더 안정한 form인 keto form으로 변환되게 되는데, 이 때 이 tautomerization에 의해 지속적으로 enol form의 pyruvate이 없어지므로 step 10의 정반응이 더욱 favorable해지게 됨.
참고로 이 때 step 6-10까지의 경우 glucose 1분자당 3탄소 분자 2개꼴의 반응이 일어나므로 실제 생산물은 2개씩이라고 생각하면 됨.
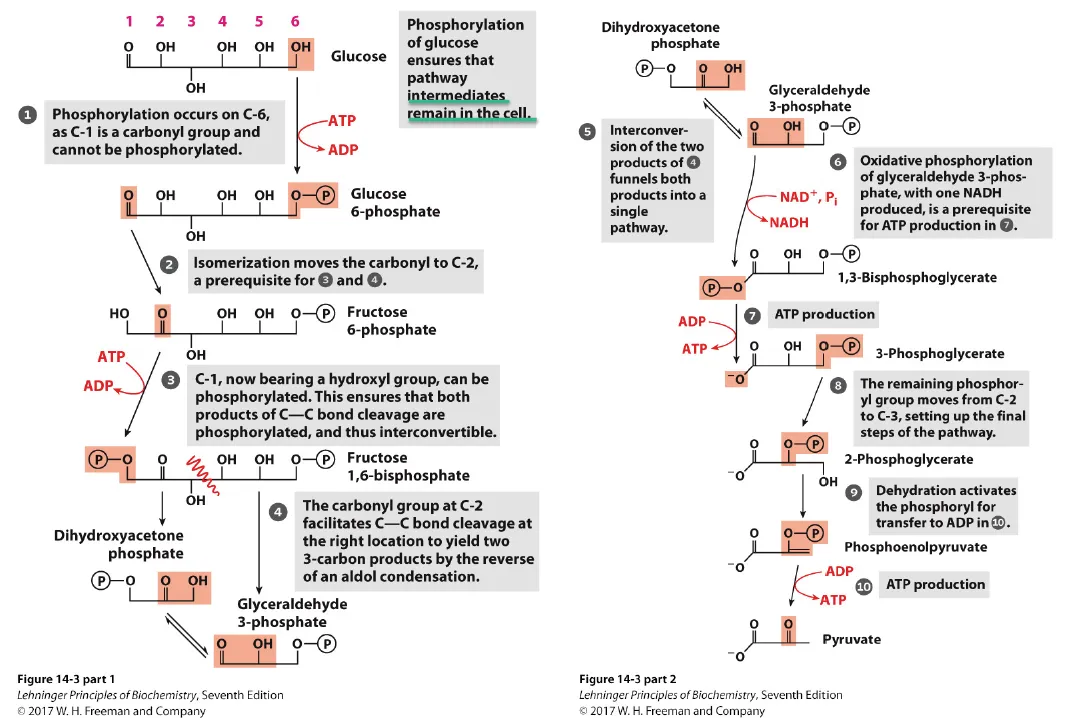
위 그림은 glycolysis의 전 과정을 정리해서 보여주고 있음. 종합해봤을 때, glycolysis의 경우 1개의 glucose, 2개의 ATP, 2개의 NAD+가 들어가서 2개의 pyruvate, 4개의 ATP, 2개의 NADH가 만들어지는 반응으로 생각할 수 있음. 한편 다음 chapter에서 더 자세히 알아보겠지만 glycolysis 반응은 상당히 tight하게 regulation되고 있음.
다음 포스트에서는 glucose 이외에 다른 monosaccharide, oligosaccharide, polysaccharide들이 glycolysis로 유입되는 방법들에 대해 알아보도록 하자.
'전공자를 위한 생물학 > 생화학' 카테고리의 다른 글
| [생화학] 13.3 : 발효(fermentation) - 1 (0) | 2025.03.25 |
|---|---|
| [생화학] 13.2 : 해당과정(glycolysis) - 5 (0) | 2025.03.25 |
| [생화학] 13.2 : 해당과정(glycolysis) - 3 (0) | 2025.03.25 |
| [생화학] 13.2 : 해당과정(glycolysis) - 2 (0) | 2025.03.25 |
| [생화학] 13.2 : 해당과정(glycolysis) - 1 (0) | 2025.03.25 |