이번 포스트부터는 ATP에 대해 알아보자.
우선 group transfer에 대해 조금 더 알아보자. 우선 매우 common하게 일어나는 transfer로 proton transfer, methyl transfer 등이 있으며, 그 밖에 fatty acid의 합성 과정에서 특히 중요한 acyl transfer, sugar와 관련되어 있는 glycosyl transfer, metabolite를 activation시키는 것과 관련되어 있는 phosphoryl transfer가 있음. 이 중 특별히 phosphoryl transfer에 대해 조금 더 알아보자.
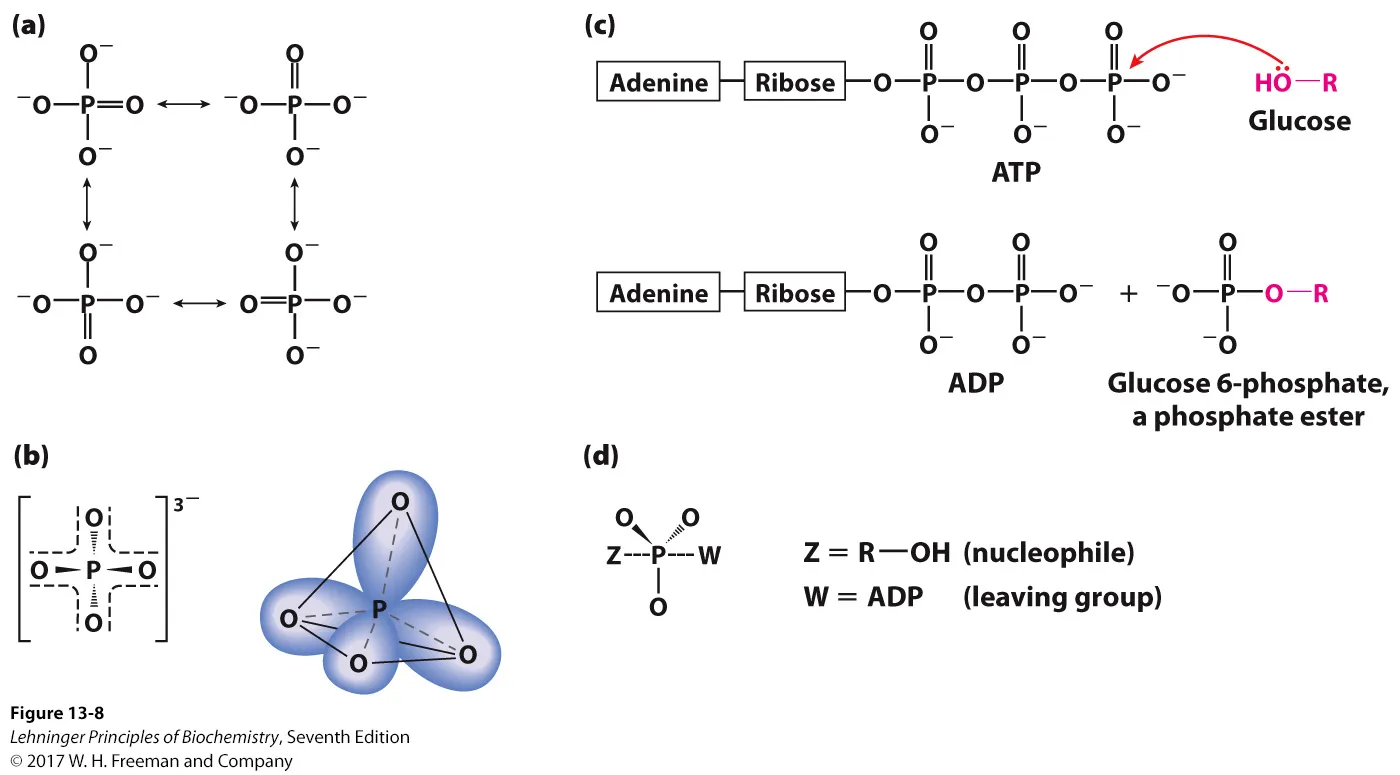
위 그림과 같이 일반적으로 ATP가 있을 때 이 ATP로부터 1개, 혹은 2개의 인산기가 분리되어서 다른 substrate로 transfer되는 것이 가능함. 그 중에서도 (c)에는 glycolysis의 첫 반응, 즉 glucose에 인산기 1개가 transfer되는 반응이 나타나 있음. 보면 glucose 끝의 OH 중 O가 nucleophilie로 작용해 ATP의 gamma phosphate를 attack하고, 그 결과 phosphoryl transfer가 일어나게 됨. 이 때, 이 반응의 중간에는 (d)와 같이, P와 5개의 원소가 공유결합으로 연결되어 있는, pentacovalent intermediate가 관찰되게 됨.
한편 isolate된 채 존재하는 phosphate를 생각해봤을 때, 이 녀석은 (a)와 같이 많은 수의 공명구조를 가질 수 있어서 상당히 안정하게 존재할 수 있음.
그렇다면 (c)에서 나타난 것과 같은 이런 transfer 반응은 어떤 의의를 가질까. 우선 poor leaving group인 OH를 good leaving group인 phosphate로 교체해준다는 것에 의의가 있음. 즉, 다음 반응이 잘 일어날 수 있게끔 intermediate들을 activation시키는 효과가 있는 것. 참고로 이 때 phosphate group의 transfer에 관여하는 enzyme들을 통틀어 kinase라 부름. (e.g. hexokinase, protein kinase C 등)
다만 이 때 주의해야 할 것이 있는데, ATP 가수분해 반응에 의한 energy가 독립적으로 다른 반응에 전달되는 것이 아니라, 두 반응이 coupled되어있으므로 ATP 가수분해에 의한 phosphate가 반응물에 전달되는 것이라는 것임.
이 때 ATP의 가수분해반응이 왜 이렇게까지 exergonic할까.
→ 우선, negative charge를 띄고 있는 phosphate들 중 하나, 혹은 두 개가 분리되게 될 시 internal electrostatic repulsion이 완화되어서 조금 더 안정적으로 변하는 것도 이유가 될 수 있고, 그 밖에, 가수분해에 의해 생성된 pi가 앞서 본 것처럼 resonance structure를 가져 안정화되는 것도 이유가 될 수 있음. 이 외에 product가 더 잘 solvation될 수 있어서도 또 하나의 이유가 될 수 있음.

한편, 실제로는 위와 같이 ATP의 hydrolysis에 주변의 물이 상당히 많이 관여하게 됨. 따라서 물이라는 주변 환경도 ATP hydrolysis에 기여함.
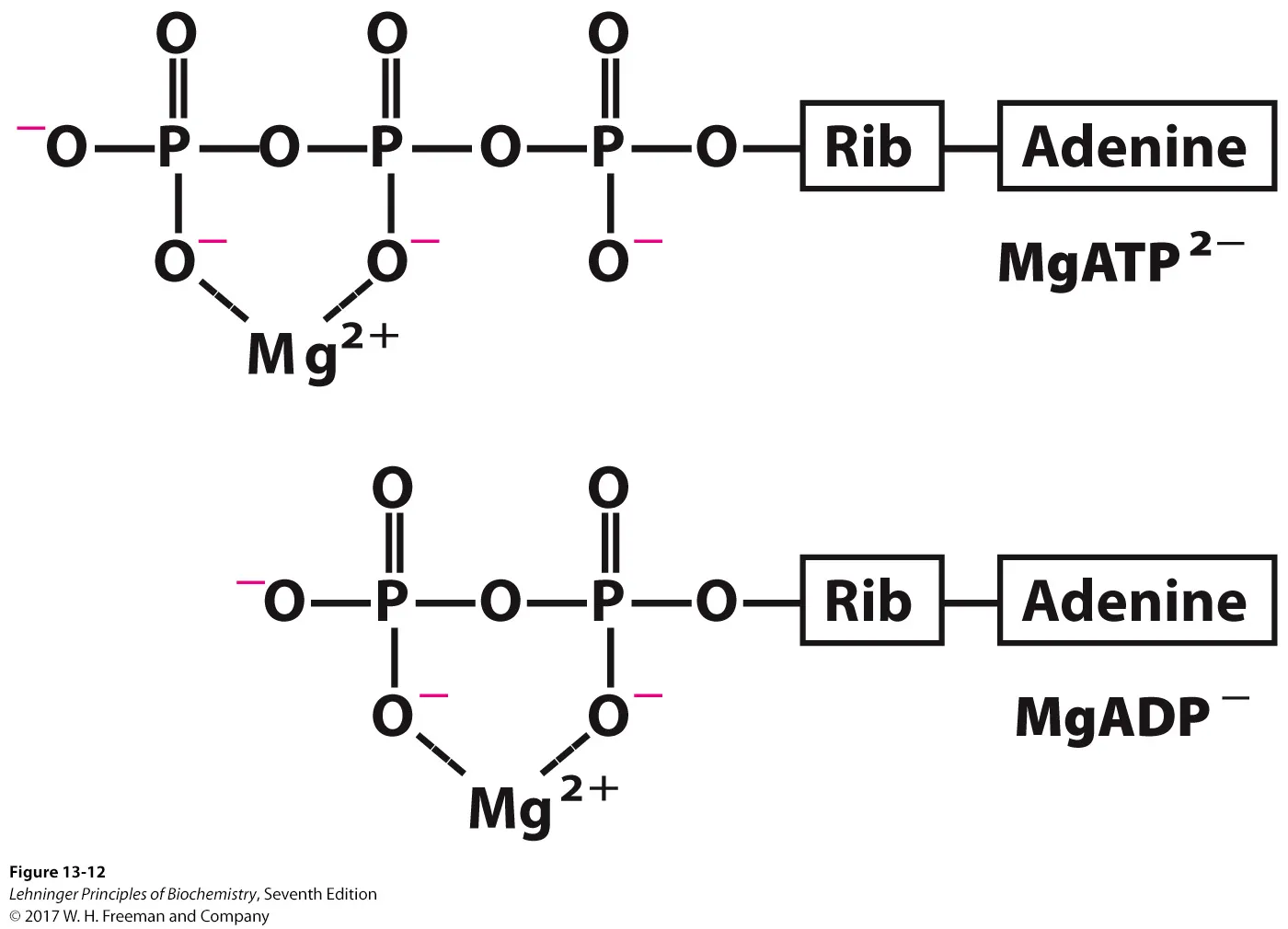
그 밖에, ATP는 위와 같이 - charge를 띄고 있기 때문에 일반적으로 Mg2+와 서로 결합한 상태로 charge를 완화한 채 많이 존재하고 있음. 따라서 우리가 흔히 알고 있는 ATP4-를 분해할 때 나오는 30.5kJ/mol의 energy가 아니라, ATP, ADP, 인산기, Mg2+의 존재에 따라서 free energy가 달라지게 되는데, 이 때의 실제 free energy를 phosphorylation potential ΔGp로 표현함.
이 ΔGp 값은 세포마다 다르고, 심지어 한 세포 내의 ΔGp도 metabolic condition이 변화함에 따라 달라질 수 있음. 이 때 일반적인 상황에서의 세포 내 ATP 농도는 equilibrium보다 상당히 높은 상태로 유지되고 있음. 따라서 결과적으로 ΔG의 절댓값이 더 커지게 됨. 그런데 대사 상태에 따라 세포 내 ATP 농도가 감소하는 경우가 발생한다면, 이 경우 ATP의 가수분해 potenty인 ΔG 절댓값도 작아지게 됨.

한편 위 table은 각종 세포에 따라서 ATP, ADP, AMP, 인산기의 농도가 어떻게 다른지를 보여주고 있음. 보면 특별히 세포 내에서 ATP의 양이 상당히 많다는 것을 알 수 있을 것임. 그 밖에, PCr로 표시되어 있는 것은 phosphocreatine으로, 이 녀석은 근육에 특히 많이 존재하며 ATP를 만들어낼 수 있음.
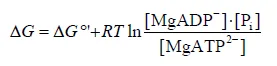
참고로 그 밖에 앞서 Mg2+의 존재에 따라서도 ΔG가 달라진다고 했었는데, 구체적으로는 위 식에 나타난 바와 같이 달라지게 됨.
다음 포스트에서 이어서 살펴보자.
'전공자를 위한 생물학 > 생화학' 카테고리의 다른 글
| [생화학] 12.3 : ATP - 3 (0) | 2025.03.25 |
|---|---|
| [생화학] 12.3 : ATP - 2 (0) | 2025.03.01 |
| [생화학] 12.2 : 생화학 반응의 화학반응적 이해 (0) | 2025.02.28 |
| [생화학] 12.1 : 생화학 반응의 열역학적 이해 - 2 (0) | 2025.02.28 |
| [생화학] 12.1 : 생화학 반응의 열역학적 이해 - 1 (0) | 2025.02.27 |