지난 포스트에 이어서 열역학과 관련된 내용에 대해 알아보자.
G의 단위는 J/mol, 혹은 cal/mol로 표현됨. 참고로 1cal=4.184J임. 이 때 ΔG가 음수이면 이 반응은 exergonic하며, 정반응이 자발적임. 한편 ΔG가 양수이면 이 반응은 endergonic하며, 이 경우 역반응이 자발적임.
그 밖에, enthalpy H는 reacting system에서의 heat content를 의미하며, 단위는 G와 마찬가지로 J/mol임. 이 때 H는 분자가 가지고 있는 화학결합의 종류, 수에 dependent하며, ΔH가 음수일 시 이 반응은 exothermic해서 반응 진행에 따라 외부로 heat이 방출되고, ΔH가 양수일 시 이 반응은 endothermic해서 주변으로부터 heat이 흡수되게 됨. 마지막으로 entropy는 무질서도의 측도이며, 단위는 J/mol K임.
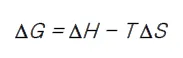
ΔG는 위와 같은 관계로 정의됨.

한편, 위 그림에 나타나 있는 것처럼 특정 반응 하에서의 ΔGo은 위와 같은 수식으로 계산될 수 있음.
이 때 ΔGo, 즉 standard free energy change는 25도(298K), 1atm 하에서 반응물, 생성물의 농도가 모두 1M일 때의 자유에너지 값을 의미함. 이 값들의 경우 이미 많이 계산되어 있음. 한편, biological reaction에서의 표준상태는 이와 조금 다를 수 있음. 예를 들어, 모든 물질이 다 1M이라면 수소이온의 농도도 1M이어야 하는데, 이 경우 pH는 0이 되어버림. 그러나 biological한 standard는 pH 7의 상태임. 이 밖에, 물의 농도는 55.5M으로, Mg2+의 농도는 1mM 정도인 것이 생물학적 스탠다드임.
따라서 나머지 조건은 모두 1M로 고정해 둔 상태에서 상기한 위 조건만 각각 다르게 setting해둔 상태로 계산한, 생물학적 의미에서의 자유에너지인 standard transformed constant ΔGo이 biochemistry에서 많이 사용됨. (이 때의 평형상수를 K'eq로 둘 수 있음. 이 때 이 값 계산에 있어서 물, 수소이온, Mg2+를 고려하지 않는데, 그 이유는 반응 전후 이들의 양이 동일하기 때문임)

위 식이 standard transformed constant change를 나타내주고 있으므로 참고할 것.

한편 위 표에는 방금의 식에 따라 K'eq를 바탕으로 ΔG'o를 계산한 결과가 나타나 있음.
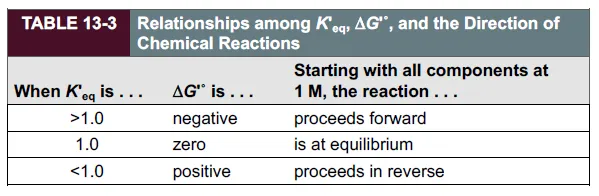
이 때 K가 1 이상일 경우 자유에너지는 음수가 되므로 반응은 자발적이게 되고, K가 1 이하일 경우 자유에너지는 양수가 되므로 반응은 비자발적이게 됨. 마지막으로 K가 1인 경우 자유에너지가 0이 되므로 equilibrium이 되고, 이런 반응의 경우 주변 조건에 따라 forward로 진행되기도, reverse로 진행되기도 함.
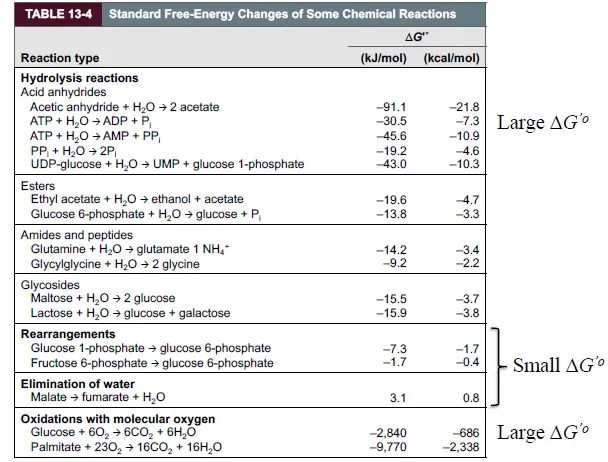
위 표에는 각종 반응의 종류에 따른 ΔG'o 값이 나타나 있음. 우선 위 표 맨 아래에 나타나 있는 glucose, palmitate들의 whole oxidation 반응의 경우 상당히 exergonic하다는 것을 알 수 있음. (oxidation 반응은 대부분 큰 자유에너지 변화를 수반하기에 정방향으로 자발적으로 일어나는 경우가 많음을 기억해두자) 그 밖에, hydrolysis reaction들의 경우에도 꽤나 exergonic함을 알 수 있음. 이 중 특히 눈여겨볼 것이 있는데, 바로 ATP에서 gamma phosphate가 떨어져나오는 가수분해반응임. 이 반응을 통해 30.5kJ/mol의 energy가 밖으로 방출됨. (즉, 7.3kcal/mol의 energy가 방출됨) 그 밖에, rearrangement, elimination of water와 같은 반응들의 경우 자유에너지의 절댓값이 꽤나 작음. 이런 반응들의 경우 어느 정도 양방향으로의 reaction이 다 가능할 수 있음.
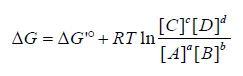
한편, 실제로는 관찰 시점에 따라, 그리고 세포 내에서의 반응물, 생성물(A, B, C, D) 농도 차이에 따라서 위 식과 같이 ΔG 값이 변할 수 있음. 한편, 이 식에서 equilibrium을 가정하면, equilibrium에서는 ΔG가 0이므로 결과적으로 앞서서 얻었던 ΔG'o에 대한 식을 얻을 수 있음.
이 때 중요한 것은, 반응의 방향은 ΔG'o이 아니라 ΔG에 의해 결정된다는 것임. 실제로 ΔG'o이 양수의 값을 가지더라도 product의 농도가 reactant에 비해 월등히 낮다면(즉, product의 즉각적인 소멸이 일어난다면) ΔG가 negative해져서 반응이 자발적일 수 있음.
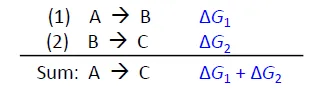
그 밖에, 위와 같이 서로 coupled된 반응이 있다면 이 둘의 summation reaction에서의 ΔG를 계산할 때 각 반응의 ΔG들을 addition할 수 있음. 이런 addition이 되기 때문에 endergonic한 반응이 exergonic한 반응과 coupling되어서 자발적으로 일어날 수 있게 되는 것임.
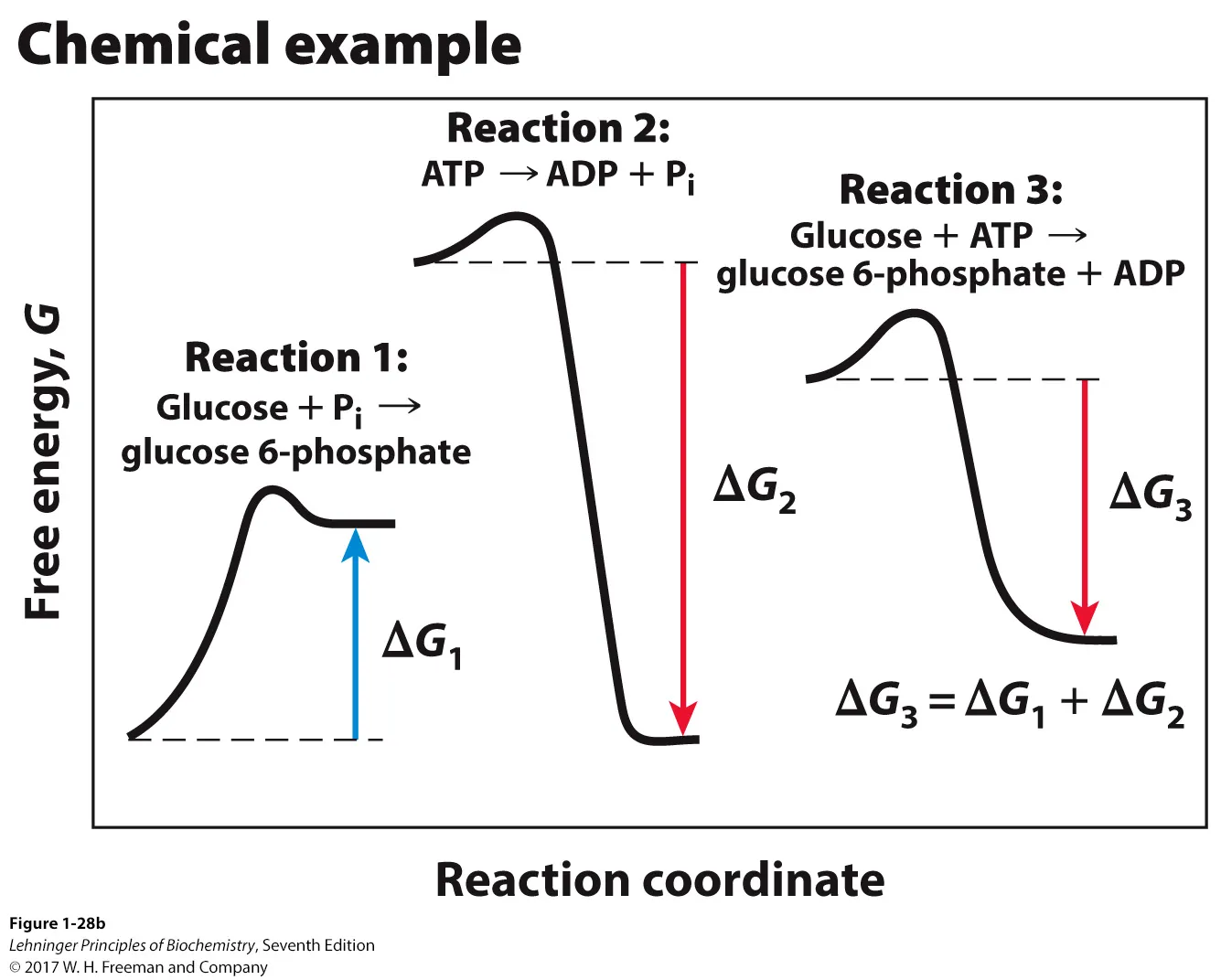
이에 대한 대표적인 예인 glycolysis의 첫 번째 step이 위 그림에 묘사되어 있음. 보면 endergonic한 glucose의 인산화반응과 exergonic한 ATP의 가수분해반응이 couple되어서 결과적으로 net reaction의 ΔG는 음수가 되게 됨.
다음으로 enzyme에 의한 catalysis에 대해 생각해보자. enzyme은 ΔG 자체는 전혀 변화시키지 않으며, 그 대신 activation free energy를 감소시켜줘서 반응속도를 더 빨라지게 만들어줌. 그 밖에, enzyme은 반응이 아주 specfic하게 일어날 수 있게끔 도와주기도 함.

실제로 위 graph와 같이 enzyme에 의해 activation barrier가 낮아지게 됨. (참고로 이 때 activation energy는 화학반응 중간에 생기는 transition state의 energy에 해당함)
다음 포스트에서는 화학반응에 대해 조금 더 알아보자.
'전공자를 위한 생물학 > 생화학' 카테고리의 다른 글
| [생화학] 12.3 : ATP - 1 (0) | 2025.02.28 |
|---|---|
| [생화학] 12.2 : 생화학 반응의 화학반응적 이해 (0) | 2025.02.28 |
| [생화학] 12.1 : 생화학 반응의 열역학적 이해 - 1 (0) | 2025.02.27 |
| [생화학] 11.5 : nuclear hormone receptor (2) | 2024.11.28 |
| [생화학] 11.4 : gated ion channel (0) | 2024.11.28 |