이번 포스트에서는 단백질을 분리하는 또 다른 방법인 전기영동(electrophoresis)에 대해 알아보자.
사실 electrophoresis의 경우 purification의 목적보다는 analytical한 목적으로 많이 사용함.
일반적으로 protein 분리시에는 polyacrylamide가 많이 사용되는데, 그러다 보니 이를 polyacrylamide gel electrophoresis(PAGE)라고 함.

위와 같이 전하가 걸려있는 영역에 단백질을 로딩 후 내릴 - charge를 많이 띄는 단백질일수록 더 빨리 가라앉고, + charge를 많이 띄는 단백질일수록 느리게 가라앉을 것임.
그런데, 사실 protein의 charge 뿐 아니라 protein의 size에 따라서도 침강 속도가 달라짐. 따라서 이 둘 중 하나에 대해서만 분리하고 싶음. 이 때 SDS(sodium dodecyl sulfate)를 사용하면 charge effect를 다 없애버릴 수 있음.

SDS는 위와 같이 생김. 이 때 dodecyl이 의미하는 것처럼 C 12개로 이루어진 소수성의 aliphatic tail이 존재하고, head 부분에는 S가 존재함. 결과적으로 이 녀석이 물에 녹을 시 - charge를 띄게 됨.
이 SDS는 protein의 표면에 uniform하게 흡착될 수 있음. 참고로 이 때 SDS 처리 전에 보통 protein을 boiling시켜서 unfolding시키게 됨(folding structure를 다 깨버림). 그 결과 native shape과는 상관없이 protein의 unfolded size 그 자체에 따라서만 분리됨.
결과적으로 small protein일 경우 조금 더 빨리 내려가고 large protein일 경우 천천히 내려감.

위 그림에 SDS를 처리할 시 일어나는 일이 나타나 있음. (보면 실제로 unfolded된 protein에 SDS가 coating되는 것을 알 수 있음)

위 그림에는 실제로 SDS-PAGE를 이용해 분리한 결과 예시가 나타나 있음.
일단 맨 왼편에는 marker의 전기영동 결과가 나타나 있음. 이 때 왼쪽 숫자는 각 marker의 molecular weight을 의미함. (작은 protein일수록 더 아래로 내려간 것을 알 수 있음)
다음으로, uninduced cell의 경우와 induced cell에 대해 살펴보자. E. coli 내부에서 induction을 시킬 수 있는 system을 많이 사용하는데, 대표적으로 IPTG를 많이 사용함. IPTG를 처리할 시 조금 더 많은 copy의 protein이 translation되게 됨. 그 결과 uninduced cell에 비해 induced cell의 경우 45,000 정도에서 상당히 굵은 band가 관찰됨.
soluble crude extract의 경우 E. coli를 다 파쇄한 후 농축시키는 과정을 거친 다음에 gel에 내려본 것임. (purification step을 거치치 않아 전체 protein이 다 들어간 것임) 그 결과 여기서도 45,000 근방에 진한 band가 나타나 있음.
이후 나와있는 ammonium sulfate를 이용해 precipitate한 sample의 경우 45,000 근처의 단백질이 가장 많은 비율로 precipitation되어 있음을 확인 가능함. (물론 약간의 inpurity가 관찰되기는 함)
그 다음에 나와있는 anion exchange, cation exchange의 결과 얻은 sample의 경우 우리가 원하는 45,000 부근의 band만이 purify된 채로 분리되었다는 것을 알 수 있음. 그 결과 거의 one band로 관찰되고 있는 것을 알 수 있음.
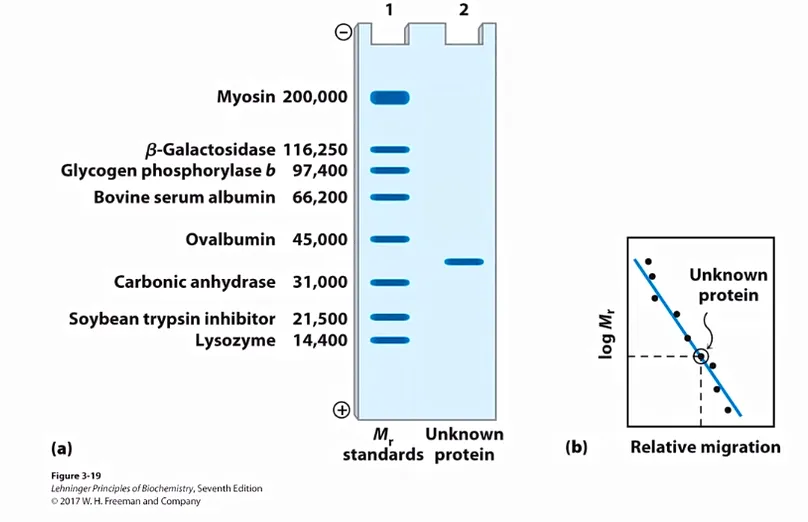
일단 이런 방식을 통해 protein을 purify했다고 하면, 이제 특정 protein의 molecular weight이 얼마나 되는지를 계산해볼 수 있음. 우선 marker band와 sample band를 비교해 대략적인 M을 유추 가능함. 보다 정확한 값을 얻기 위해서는, 오른쪽에 나와있는 graph처럼 standard curve를 그리면 됨. 이를 그릴 때에는 longM을 y축으로 두게 됨. 그 결과 얻어진 standard curve를 사용하면 unknown protein의 M 값을 비교적 정확하게 예측해볼 수 있음.
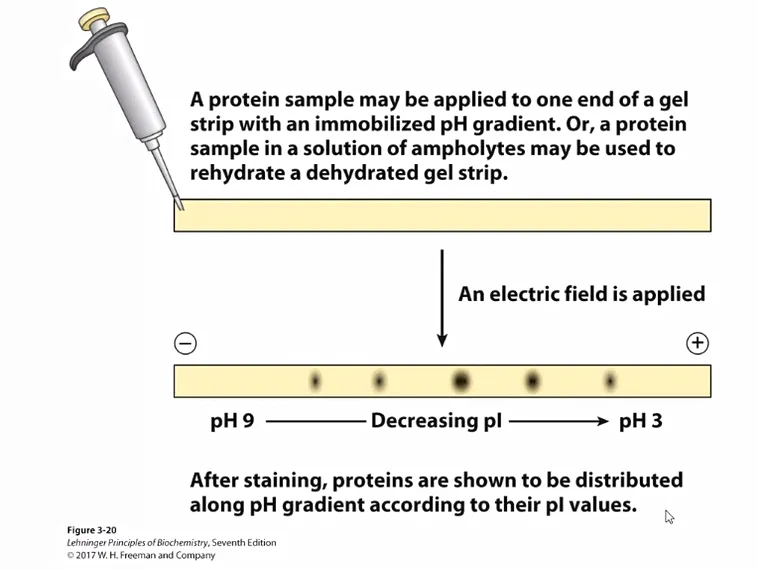
다음으로, 위 그림에는 isoelectric focusing이 나타나 있는데, 이는 protein을 pH에 따라 분리하는 기법임. 보면 위 그림의 가로 strap에 걸쳐 점차 pH가 낮아지는 식으로 buffer가 쭉 분포되어 있으며, 왼쪽에서 오른쪽으로 - → +의 전하가 걸려 있음.
이 때 protein들은 각자 쭉 strap을 따라 이동하다가, 딱 자기의 pI가 되는 pH 지점에 이르게 되면 charge를 띄지 않게 될 것임. 그 결과 이들은 여기에서(외부 전기장이 아무리 세더라도 중성이므로) 멈춰있게 될 것임. 이런 방식으로 pI에 따라 protein을 분리할 수 있음.
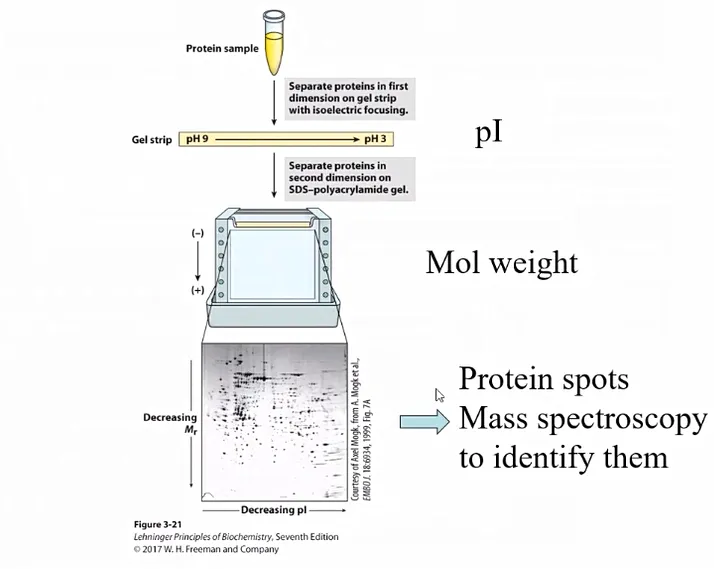
이제 isoelectric focusing과 SDS-PAGE를 합하게 되면 위와 같이 2D electrophoresis를 수행할 수 있음. 즉, 단백질의 pI와 molecular weight에 따라서 protein을 정교하게 분리할 수 있음.
그 결과 얻어진 protein spot을 따서 mass spectroscopy를 수행할 수 있음. (이 spot에는 하나의 protein이 있을 수도, 여러개의 protein이 있을수도 있으므로 이를 MS로 확인)
한편 실험 전에 선험적으로 알고 있었던 protein의 charge와 크기정보 등을 통해 unknown protein이 어느 spot 즈음에서 나올지를 미리 예상하고, 더 정밀하게 확인하는 것 또한 가능함.
결과적으로 2D gel electrophoresis 등을 통해 알아낸 특정 protein의 pI, size 등을 바탕으로 chromatography를 이용해서 그 protein을 purify할 수 있음. 이후 비로소 이 녀석을 sequencing할 수도 있음.
그 밖에 purify된 protein을 가지고 구조 분석을 하거나, NMR을 찍는 등의 일도 가능함.
다음 포스트에서는 단백질의 농도를 재는 방법, 그리고 단백질의 활성도에 대해 알아보자.
'전공자를 위한 생물학 > 생화학' 카테고리의 다른 글
| [생화학] 2.8 : 단백질 시퀀싱(protein sequencing) (0) | 2024.11.04 |
|---|---|
| [생화학] 2.7 : 단백질의 농도, 단백질의 활성 (0) | 2024.11.04 |
| [생화학] 2.5 : 컬럼 크로마토그래피(column chromatography) (3) | 2024.11.04 |
| [생화학] 2.4 : 단백질 관련 실험기법들 - 2 (0) | 2024.11.04 |
| [생화학] 2.4 : 단백질 관련 실험기법들 - 1 (0) | 2024.11.04 |