지난 포스트에 이어서 알아보자.
이전 포스트에서는 Fructose-2,6-bisphosphate(F2,6BP)에 대해 잠시 언급되었음. 이 녀석은 도대체 어떤 녀석일까.

위 그림의 왼쪽에 나타나 있는 것이 F2,6BP의 구조임. 오른쪽의 F1,6BP 구조와 비교해보면, 한 인산기의 위치가 1번탄소가 아닌 2번탄소임을 알 수 있음. F2,6BP는 어떤 대사과정의 중간체로 작용하지 않으며, 오로지 regulation하는 역할만을 수행함.

위 graph를 보면 알 수 있는 것처럼, 실제로 F2,6BP는 PFK-1에 대해서는 activator로 작용하고, FBPase-1에 대해서는 inhibitor로 작용함. 결과적으로 F2,6BP가 많을 시 glycolysis가 촉진됨.

한편 F2,6BP는 위와 같은 과정에 의해 생성됨. 보면 F6P가 PFK-2에 의해 F2,6BP로 변할 수 있고, 한편 F2,6BP는 FBPase-2에 의해 다시 F6P로 돌아올 수 있음.
그런데 이 때 등장하는 PFK-2, FBPase-2는 매우 흥미로운 특성을 가지고 있음.
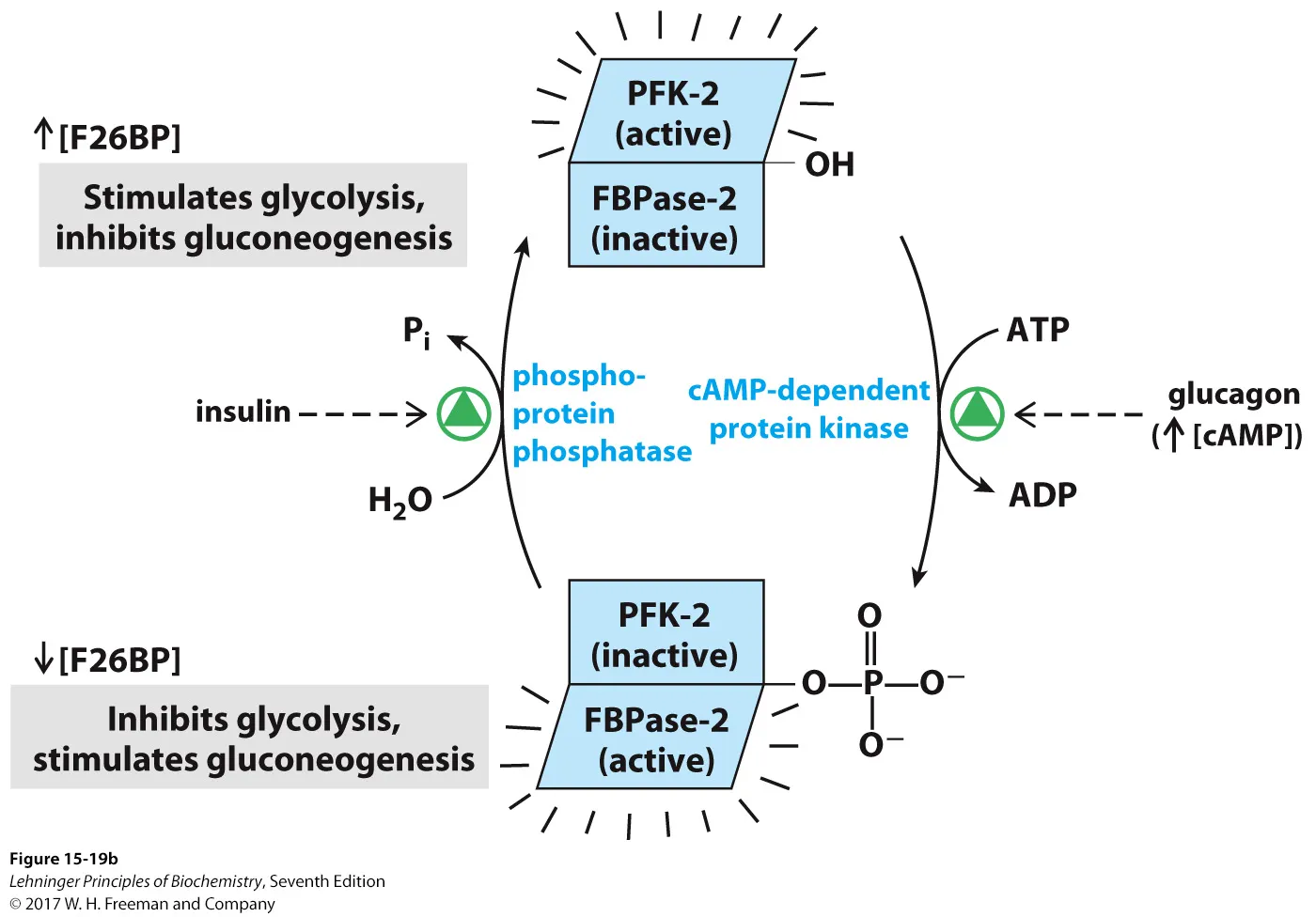
이 두 효소는 위 그림상에도 나타나 있는 것처럼 같이 붙어서 single protein의 형태로 존재함. 그리고, 한 녀석이 activation되어있을 때는 다른 녀석이 inactivation된다는 것을 알 수 있음.
우선 cAMP-dependent protein kinase(PKA로 생각하면 편함)가 이 단백질에 작용해서 OH기에 인산기를 붙여줄 시 PFK-2가 inactive해지고 FBPase-2는 active해짐. 한편 phosphoprotein phosphatase가 작용해 인산기를 떼서 ADP로 옮겨주게 되면 그 결과 PFK-2는 active해지고 FBPase-2는 inactive해짐.
이 때 insulin은 phosphoprotein phosphatase를 activation시켜서 결과적으로 PFK-2를 active하게 만들어주고, 그럴 시 F2,6BP가 많아져서 glycolysis가 촉진되게 됨. 한편 glucagon은 Gα signaling에 의해서 cAMP-dependent protein kinase를 활성화시키게 되고, 그럴 시 FBPase-2가 활성화되어서 F2,6BP의 양이 적어지게 됨. 그 결과 glycolysis 반응은 많이 일어나지 않고, 그 대신 많아진 F6P가 gluconeogenesis를 통해 glucose의 형태로 합성되어 blood 상으로 나가게 됨.

한편 앞서 PPP에 대해 배울 때, ribulose 5-phosphate가 ribose 5-phosphate epimerase에 의해 Xylulose 5-phosphate로 바뀔 수 있고, 이 녀석이 많아질 시 nonoxidative phase가 많이 일어난다 했었음. 이 때 Xylulose 5-phosphate는 사실 앞서 봤던 phosphoprotein phosphatase를 allosterically active할 수도 있음. 그 결과 F2,6BP의 양이 많아지게 되고 glycolysis 반응은 촉진되는 한편 gluconeogenesis 반응은 억제되게 됨.
한편 촉진된 glycolysis의 결과로 acetyl-CoA의 양이 늘어날 것임. 더불어 PPP가 많이 일어날 시 NADPH의 양도 늘어남. 그런데 acetyl-CoA와 NADPH는 fatty acid synthesis에 있어 매우 핵심적인 녀석들임. 따라서 이런 반응들의 결과로 fatty acid synthesis도 촉진되게 됨.
다음으로 pyruvate kinase에 대해 일어나는 regulation 과정에 대해 알아보자.
pyruvate kinase는 F1,6BP에 의해 allosteric하게 activation될 수 있음. 그 결과 glycolysis가 더 많이 일어나게 됨.

한편 pyruvate kinase에는 L form(liver pyruvate kinase)과 M form(muscle pyruvate kinase)의 두가지 isozyme이 있음. (이들 둘의 amino acid는 다르지만, 같은 효소반응을 매개하므로 이들을 isozyme으로 볼 수 있는 것) 이 중 L form만이 위 그림 왼쪽에서와 같이 인산화에 의해 조절될 수 있음. 그런데 L form의 pyruvate kinase가 PKA에 의해 인산화될 시 이 녀석은 inactive해짐. (그리고 PKA의 이러한 반응은 glucagon이 촉진할 수 있음) 한편 이 녀석이 phosphatase에 의해 탈인산화되면 비로소 active한 L form pyruvate kinase가 되는 것임. (이러한 인산화에 의한 조절은 M form에서는 일어나지 않음)
한편 활성화된 pyruvate kinase 또한 다양한 factor들에 의해 allosteric regulation될 수 있음. 우선 이 녀석은 glucose가 풍부하다는 indicator인 F1,6BP에 의해 activation될 수 있음. 한편 이 녀석은 energy가 충분하다는 indicator인 ATP, acetyl-CoA, long-chain fatty acids 등에 의해 inhibition될 수 있음. 그 밖에 이 녀석은 pyruvate가 transamination에 의해 변해서 생기는 alanine에 의해서도 inhibition될 수 있는데, 결국 alanine은 pyruvate의 양을 indicate해주는 역할을 하므로 이 inhibition은 make sense함.
다음 포스트에서 이어서 살펴보자.
'전공자를 위한 생물학 > 생화학' 카테고리의 다른 글
| [생화학] 14.3 : glycogen 대사 - 1 (0) | 2025.03.26 |
|---|---|
| [생화학] 14.2 : glucose 대사 조절 - 4 (0) | 2025.03.26 |
| [생화학] 14.2 : glucose 대사 조절 - 2 (0) | 2025.03.26 |
| [생화학] 14.2 : glucose 대사 조절 - 1 (0) | 2025.03.26 |
| [생화학] 14.1 : 대사 조절 개론 (0) | 2025.03.26 |