이번 포스트에서는 지난 포스트에 이어서 산화-환원반응에서 핵심적인 식인 네른스트 방정식(Nernst equation)을 포함한 개념들에 대해 살펴보자.
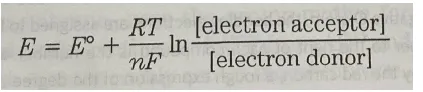
한편, 실제 상황에서의 E, 즉 에너지 준위는 위와 같은 Nernst equation을 통해 계산할 수 있음. 이 때 n은 molecule당 transfer되는 electron의 수를 의미하고, F는 Faraday constant를 의미함.

그리고 T를 298K(=25도)으로 가정한 뒤 식을 세워볼 시 위와 같은 식을 얻어낼 수도 있음.

그리고 ΔE'◦는 위와 같이 계산함. 이 때, 말 그대로 전자를 받는 녀석의 reduction potential 값에서 전자를 주는 녀석의 reduction potential 값을 빼면 됨. (별다른 부호변환을 하면 안됨)

그러면 결국 이렇게 구한 값을 이용해 위 식과 같이 ΔE'◦를 구할 수 있음.
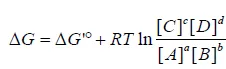
그리고 결국 reactant와 product들의 농도를 알고 있다면 위 식을 이용해 ΔG값까지 계산할 수 있음.
상당히 많은 biochemical oxidation-reduction reaction에서는 two electron이 전달됨. 그 밖에, 많은 dehydrogenase의 경우 proton의 transfer, 혹은 hydride의 transfer 반응을 촉매하는 경우가 많음.
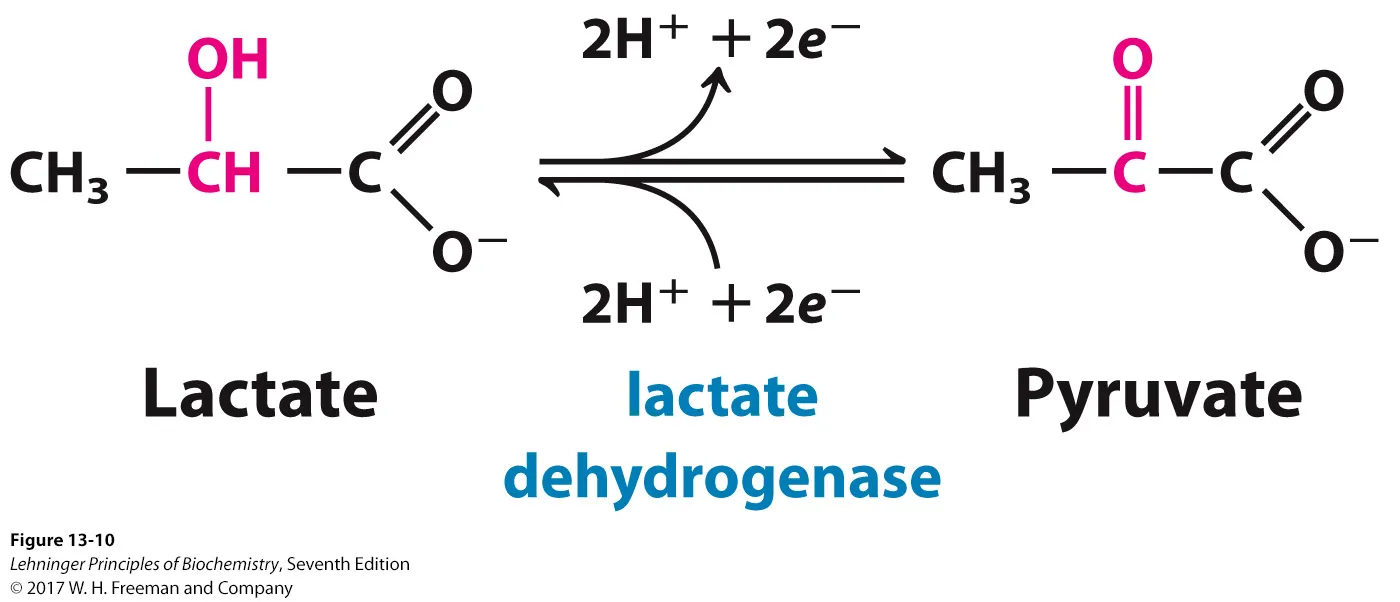
위 그림에 나와있는 반응은 pyruvate가 lactate가 되는 반응인데, 이 반응에서도 2개의 전자와 2개의 proton이 들어가는 것을 알 수 있음.
다음으로 common한 redox cofactor 중 하나인 NAD와 NADP에 대해 알아보자. 이들은 electron 2개씩을 한번에 받아들이며, reaction이 진행되는 동안 enzyme에 transient하게 붙어있다가, 이후에는 다시 dissociate될 수 있음. 일반적으로 이들에게 전자 2개를 제공해줄 때, hydride ion이 많이 이용됨.
한편 NAD+, NADP+에서 +는 net charge를 의미하는 것이 아님. 그 대신 N이 oxidize form임을 indicate하는 표시임.
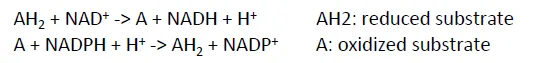
위 반응식에는 이들과 관련된 반응이 나타나 있음.
한편, NAD, NADP는 dehydrogenase의 Rossman fold에 loose하게 binding하게 됨. 따라서 때때로 이들은 다른 enzyme으로 옮겨갈 수 있음. 그 밖에 NAD, NADP는 allosteric regulator로도 가능함.
NAD, NADP는 Niacin이라는 vitamin으로부터 만들어짐. 그리고 Niacin은 Tryptophan에서 만들어짐. 그러나 사람은 충분한 양을 합성하지 못함. 따라서 Tryptophan이 낮은 음식을 주식으로 섭취하는 사람들, 예를 들어 maize를 주식으로 섭취하는 남미 사람들의 경우에는 niacin이 부족해서 Pellagra가 발생할 수 있음. (Pellagra가 발생할 시 dermatitis, diarrhea, dementia 등의 증상이 나타날 수 있음) 그 밖에 알콜 중독의 경우에도 niacin이 부족해져서 Pellagra와 유사한 증상이 나타날 수 있음.

위 그림에는 NAD+의 구조가 나타나 있음. 이 때 NAD 중 위쪽 base 부위에 2개씩의 전자와 proton이 들어가게 될 시 NADH의 구조가 만들어지게 됨. (이 과정에서 이중결합 한 개가 사라짐) 그 밖에, 위 그림상에서 왼쪽 아래에 해당하는 당 구조 중 2번 탄소에 붙은 OH 대신 phosphate가 esterified되어있는 경우에는 NADP+가 됨.
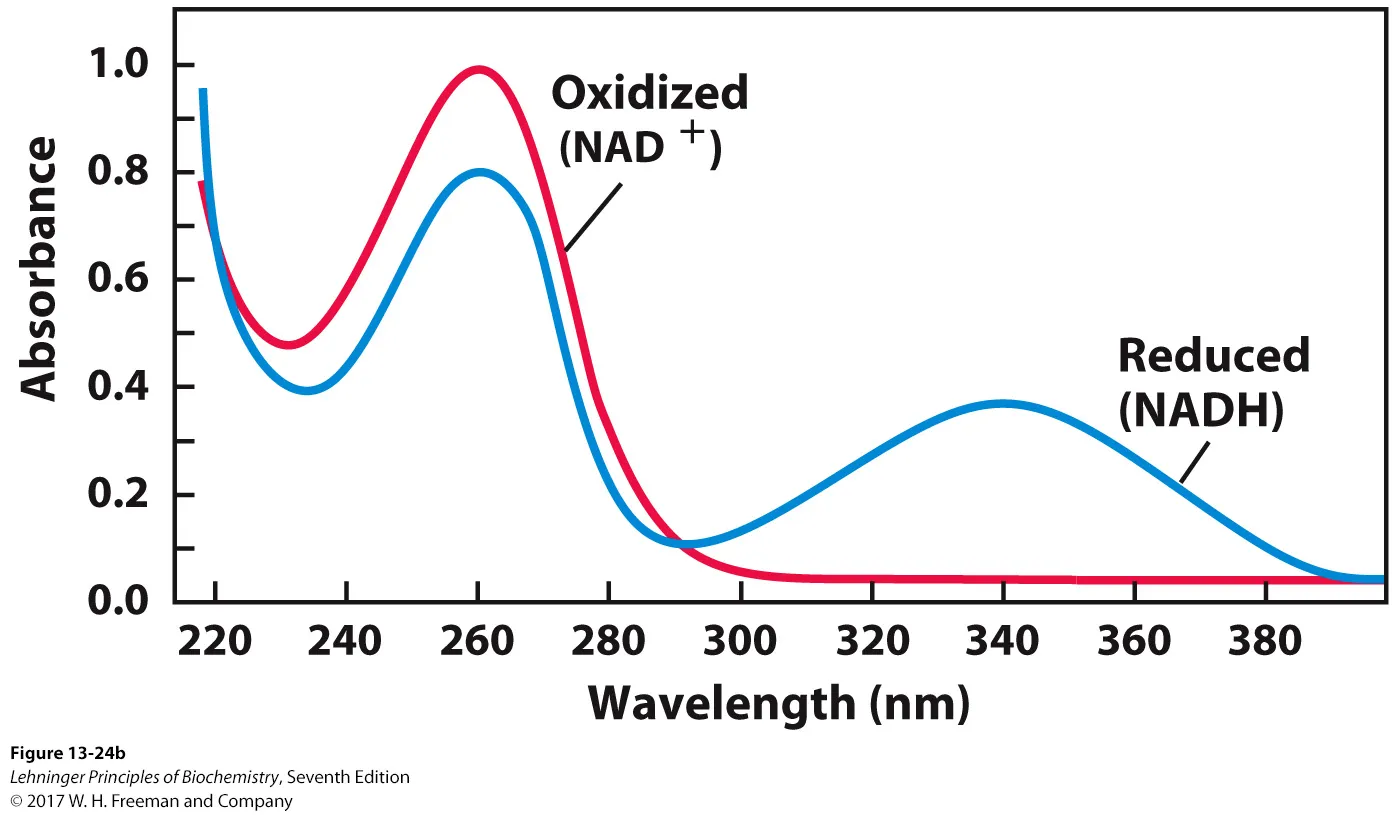
한편, 흥미롭게도 UV-spectrophotometry 상에서 NAD+와 NADH의 흡수 파장대가 위와 같이 다르므로, spectrum 변화를 측정할 시 NADH의 농도를 측정할 수 있음.
다음으로 FMN(flavin mononucleotide)과 FAD(flavin adenine dinucleotide)에 대해 알아보자. 이들은 vitamin riboflavin에서 유래되었으며, 애초에 전자를 두 개밖에 받을 수 없는 NAD, NADP와는 달리 이들은 전자를 한 개 받을수도, 2개 받을수도 있기에 보다 다양한 반응에 관여 가능함. 이 때 fully reduced form을 FMNH2, FADH2로, 전자를 1개 받았을 때의 form은 FMNH·, FADH·으로 표시할 수 있음. 이 경우에도 마찬가지로 reduction 상태에 따라서 흡광도의 maximum이 변화하는데, 2개의 전자를 가지고 있는 경우 360nm, 1개의 전자를 가지고 있는 경우 450nm, fully oxidized된 경우 370, 440nm에서 흡광하게 됨.
FMN, FAD의 경우 단백질에 단단히 결합하는 prosthetic group으로, 심지어 succinate dehydrogenase의 경우 FAD가 covalently bonded된 채로 관찰됨.
한편 지금까지 살펴본 cofactor들의 reduction potential은 binding하는 단백질에 따라서 달라지게 됨.
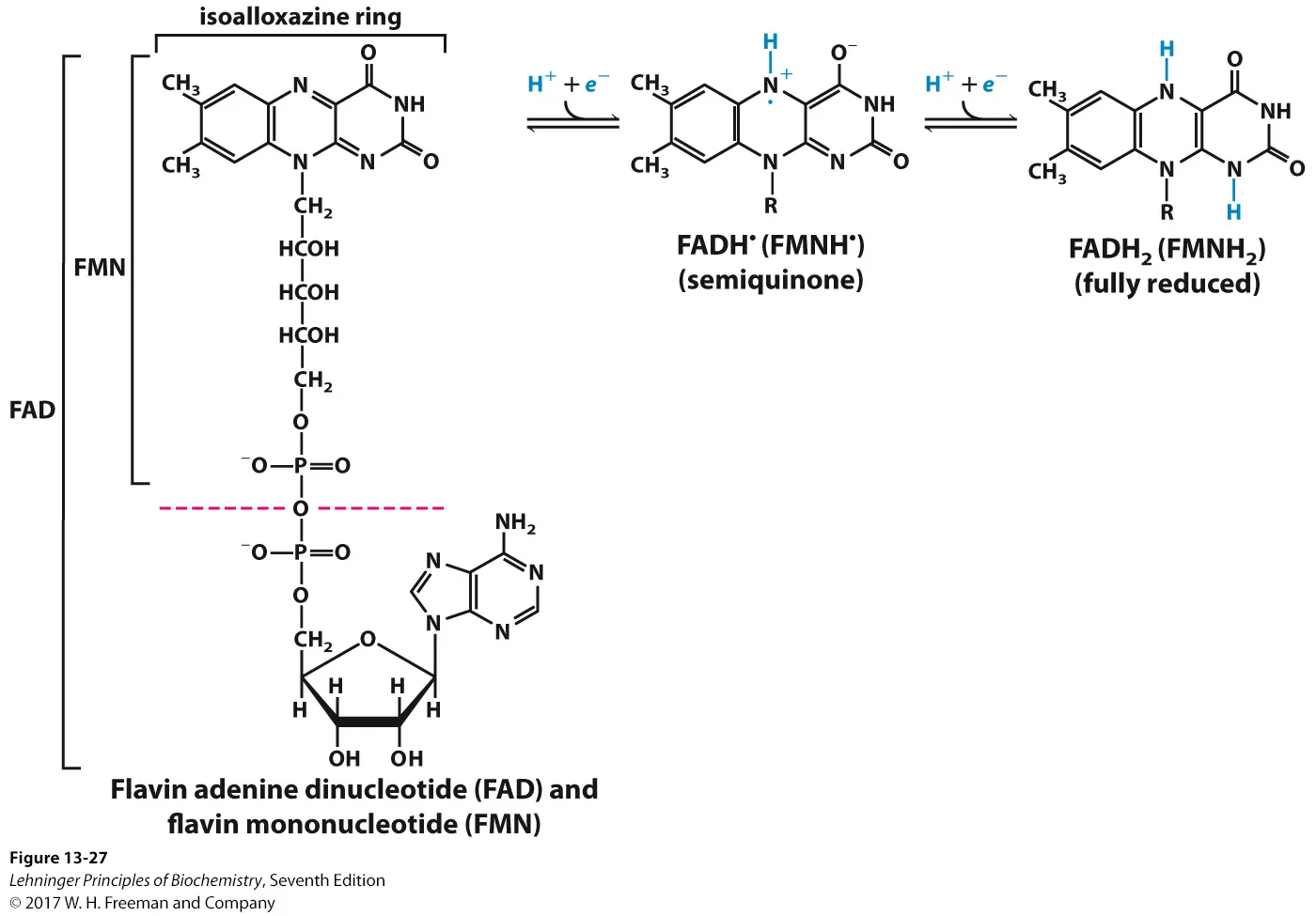
위 그림상에 FMN, FAD의 구조가 각각 나타나 있음. 이들의 경우 위쪽에 있는 isoalloxazine ring이 전자를 1개 받아 semiquinone이 될 수도, 전자를 2개 받아 fully reduced form이 될 수도 있음.
다음 포스트부터는 이제 본격적으로 해당과정(glycolysis)에 대해 알아보도록 하자.
'전공자를 위한 생물학 > 생화학' 카테고리의 다른 글
| [생화학] 13.2 : 해당과정(glycolysis) - 1 (0) | 2025.03.25 |
|---|---|
| [생화학] 13.1 : 당 대사 개론 (0) | 2025.03.25 |
| [생화학] 12.4 : 산화-환원 반응 - 1 (0) | 2025.03.25 |
| [생화학] 12.3 : ATP - 3 (0) | 2025.03.25 |
| [생화학] 12.3 : ATP - 2 (0) | 2025.03.01 |