이번 포스트에서는 진핵생물에서의 전사 조절 과정에 대해 대략적으로 알아보자.
진핵생물에서 전사 조절은 주로 initiation step에서 일어남. 그런데 어떤 경우에는 elongation에서 전사 조절이 이뤄지기도 함. 가장 대표적인 것이 transcription pausing 혹은 transcription arrest인데, 쉽게 말해 전사가 쭉 진행되다가 갑자기 멈춰버린 채로 존재하며 전사가 억제되는 현상임.
대표적인 예가 초파리의 Hsp70 gene인데, 이 gene은 평소에는 전사되지 않고 있다가 heat shock이 오면 즉각적으로 전사되어야 할 필요가 있음. 이 때 transcription pausing이 활용되는데, heat shock이 없을 때 Hsp70 gene은 처음에 어느 정도 전사되다가 중간 지점에서 pausing하고 있음. 그러다가 heat shock이 있으면 비로소 전사가 즉각적으로 재개되고, 그 결과 Hsp70이 만들어짐. 이 때의 pausing 현상을 promoter proximal pausing이라 불러줌.
이런 pausing은 특정 pause site가 존재해서 그곳에서 일어나기도 하고, DNA sequence와 새로 합성된 RNA간의 hybrid가 불안정해서 생길 수도 있음. 후자의 경우 pause가 일어난 후 다시 backtracking이 일어나 RNA 수선을 거치게 됨. 이에 대해 뒤에서 다시 알아볼 것임.
그러면 promoter proximal pausing에 대해 조금 더 자세히 알아보자. promoter proximal pausing은 specific한 pause site에 의해 일어나며 이 site는 전사개시부위로부터 대략 20~50bp downstream에 위치함.
promoter proximal pausing에는 DRB sensitivity inducing factor(DSIF)와 negative elongation factor(NELF) 등의 단백질들이 사용되며 pausing되어 있던 RNA polymerase II를 다시금 elongation하게 해주는 protein에는 positive elongation factor-b(P-TEFb)가 있음. (P-TEFb는 RNA polymerase II, DSIF, NELP를 인산화시켜줌)
다음으로 앞서 잠시 언급했었던 proofreading에 대해 살펴보자. class II gene의 전사 과정에서의 proofreading에는 TFIIS라는 subunit이 관여함. (조금 더 엄밀히 표현하자면 TFIIS가 proofreading을 촉진시킴)

이와 관련된 실험 결과를 살펴보자. 이 때 graph의 가로축은 시간, 세로축은 전사의 진행정도(전사의 재료로 들어가는 GMP를 labeling 후 이 녀석의 농도를 측정)를 나타냄. 시간축을 보면 맨 처음에는 DNA와 RNA polymerase II, NTP를 넣어준 후 1분 시점에 Heparin을 넣어줌. 이 때 heparin은 polyanion으로, - charge를 띄는 녀석들이 여러 개 결합하고 있는 형태임.
그런데 DNA, RNA에 붙는 RNA polymerase II의 경우 DNA, RNA와 더 잘 붙기 위해 binding site에 + charge를 띄는 amino acid들을 가지고 있음. 이 때문에 heparin을 넣어주게 되면 heparin이 RNA polymerase II의 DNA, RNA binding site에 붙어버림. 결과적으로 heparin에 의해 block된 RNA polymerase II들은 새롭게 전사를 시작하지 못함. 물론 heparin이 첨가되기 전부터 전사가 시작된 경우 heparin 유무와 관계없이 전사를 지속할 수 있음. (특히 RNA polymerase II의 경우 processivity를 가지므로 일단 한 번 붙어서 전사가 시작되고 나면 전사가 종결되기 전까지는 계속 붙은 채로 전사를 이어나감)
이후 2.5분 시점에 드디어 TFIIS protein을 넣어줘봄. 위 graph에는 사실 2.5분 시점에서도 TFIIS를 넣지 않은 경우(파란색)와 2.5분 시점에 TFIIS를 넣은 경우(빨간색)가 동시에 나타나 있음. 보면 TFIIS를 넣어준 경우 전사가 더 잘 일어남. 이를 통해 TFIIS가 어떤 식으로든 전사를 효율적으로 일어나게 해 준다는 것을 알 수 있음. (참고로 이와는 별개로 맨 처음부터 TFIIS를 넣은 채 동일한 실험을 수행해 봤는데, 결과적으로 위 그림과 별 차이가 없었음. 이를 통해 TFIIS가 initiation에는 거의 관여하지 않고 elongation에 관여한다는 것을 알 수 있음)

이후 수많은 연구를 통해 실제로 TFIIS가 위와 같이 기능한다는 것을 알아냄. 보면 mismatched RNA를 발견하거나 혹은 불안정한 RNA-DNA hybrid를 발견하면 backtrack이 일어남. 그러면 backtrack에 의해 RNA의 3' 말단이 바깥쪽으로 노출됨. 이 때 TFIIS가 작용하는데, TFIIS가 RNA polymerase II의 RNase activity를 확 증대시켜주게 됨. 이 결과 노출된 3' RNA 말단이 제거되고, 다시금 전사가 재개됨.
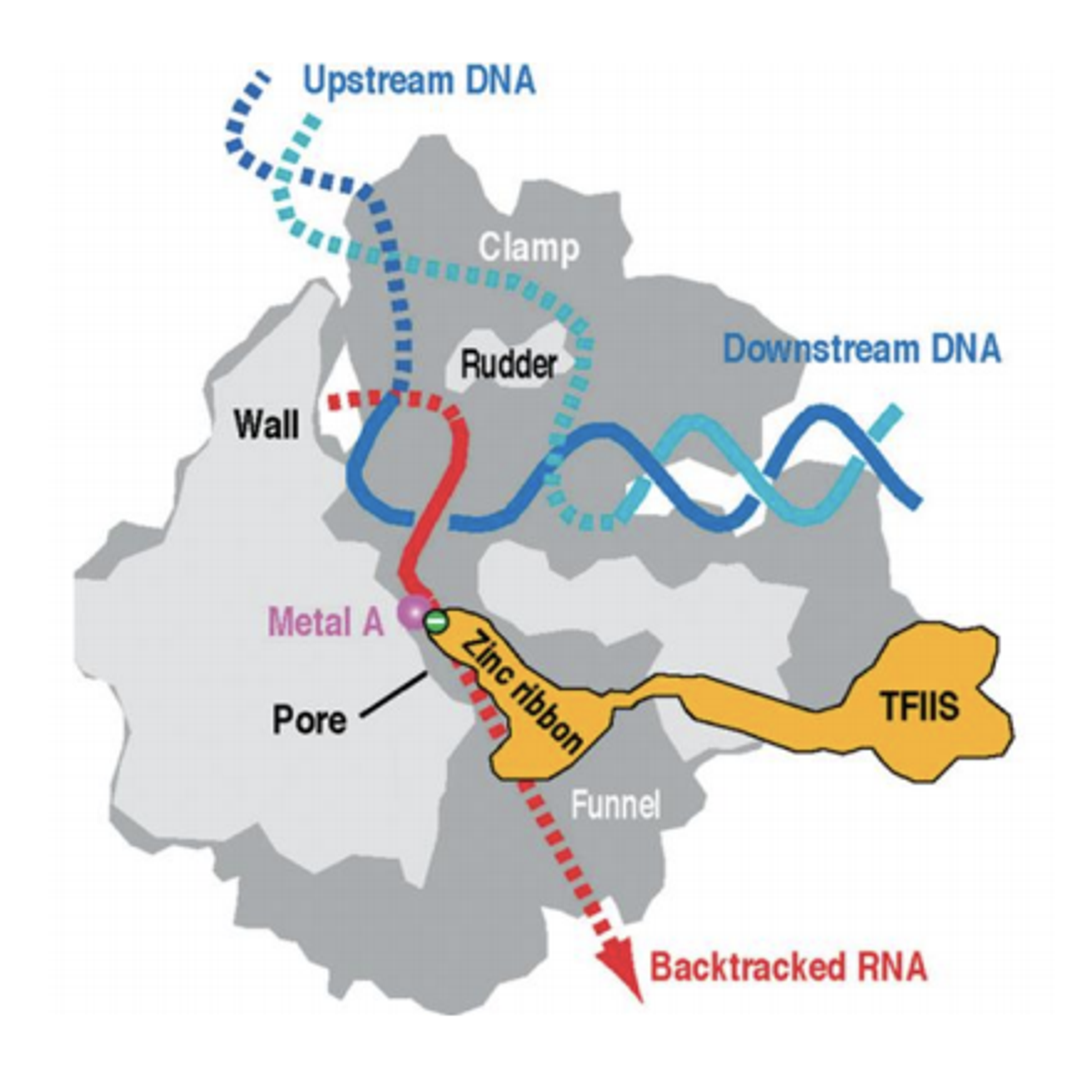
그 후 구조생물학적 연구들을 통해 위와 같이 TFIIS의 구조를 얻는데 성공함. 보면 TFIIS의 끝 부분, 즉 Zinc ribbon 끝부분에 Zinc가 위치하고 있음. 그런데 이 Zinc가 딱 차지하게 되는 공간이 metal B site임. metal B site에 들어올 metal B는 원래는 substrate와 함께 들어오고, substrate 구조 안정화에 의해 metal B도 metal B site에 들어가게 됨.
그런데 이 자리를 TFIIS의 Zinc가 대신 차지하게 되고 결과적으로 RNA polymerase II로 하여금 강한 RNase activity를 가지게끔 함. (이것은 직관적으로도 make sense하는데, 원래 substrate와 함께 채워져야 할 metal B site가 substrate 없이 그냥 채워지게 되면 RNA polymerase II가 합성되었던 RNA 일부를 분해하는 활성을 가지게 되는 것이 자연스러움. 혹은 그냥 metal A, B가 차서 RNA를 합성하는 활성이 생길 수 있는 것처럼 metal A, B가 차서 RNA를 분해하는 활성 또한 생길 수 있다고 이해해도 됨)
다음 포스트에서는 rRNA 유전자의 전사를 위해 중요한 class I factor들에 대해 알아보도록 하자.
'전공자를 위한 생물학 > 분자생물학' 카테고리의 다른 글
| [분자생물학] 11.7 : class III factors (0) | 2023.12.17 |
|---|---|
| [분자생물학] 11.6 : class I factors (0) | 2023.12.17 |
| [분자생물학] 11.4 : TFIIH의 구조와 기능 - 2 (0) | 2023.12.17 |
| [분자생물학] 11.4 : TFIIH의 구조와 기능 - 1 (0) | 2023.12.17 |
| [분자생물학] 11.3 : TFIIB의 구조와 기능 (0) | 2023.12.17 |