콜로니 PCR의 트러블슈팅을 위한 팁
콜로니 PCR은 빠르고 간편한 실험이지만, 가끔 예상치 못한 오류나 헷갈리는 결과가 나올 때가 있어요.
이번 글에서는 PCR이 실패했을 때 원인 찾기, 위양성/위음성 줄이기, 클로닝 확인 정확도 높이기 같은 현실적인 팁들을 알려드릴게요.
밴드가 안 떠요! 왜 그럴까요?

콜로니 PCR을 돌렸는데, 겔에 아무것도 안 보인다면 당황할 수 있죠. 가장 흔한 원인은 아래와 같아요.
PCR 효소의 성능 저하
Taq polymerase는 실온에서 오래 두면 성능이 떨어져요.
새로 꺼낸 Taq으로 다시 실험해보면 문제 없이 뜨는 경우도 있어요.
세포가 충분히 파쇄되지 않음
콜로니를 너무 작게 떼었거나, 파쇄 시간이 짧을 수 있어요.
첫 95도 변성 단계에서 5~10분 정도 더 길게 잡아보세요.
또는 콜로니를 PCR 하기 전에 살짝 끓이거나(boiling method), lysis buffer로 먼저 처리하는 방법도 있어요.
프라이머 결합 실패
프라이머의 Tm(녹는점)이나 위치가 적절하지 않을 수 있어요.
프라이머가 유전자 양쪽에 잘 걸쳐 있는지, GC 함량이 너무 낮거나 높지는 않은지 확인해 보세요.
밴드가 나왔는데도 이상해요
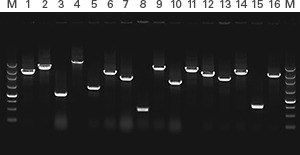
밴드가 나왔는데, 예상한 크기랑 다르거나, 여러 개의 밴드가 나오는 경우도 있어요.
비특이적 증폭
Taq이 비슷한 서열에서도 PCR을 할 수 있어요.
이럴 땐 annealing 온도를 조금 높여보거나, 프라이머 농도를 조절해보세요.
프라이머를 더 특이적으로 다시 설계하는 것도 좋은 방법이에요.
벡터 단독 증폭 vs. 삽입 유전자 포함 증폭
클로닝이 안 된 클론에서도 PCR이 될 수 있어요.
예를 들어, promoter와 유전자 내부를 잇는 프라이머를 쓰면 삽입된 경우에만 밴드가 뜨죠.
반대로 MCS 바깥쪽 프라이머만 쓰면, 삽입 유무와 관계없이 밴드가 나올 수도 있어요.
따라서 항상 negative control(삽입 안 된 벡터)도 밴드를 내릴 때 함께 내려보는 게 좋아요!
위양성과 위음성을 피하려면?
위양성(false positive)
클로닝이 안 됐는데, PCR에서 밴드가 나오는 경우
→ 프라이머 위치와 설계를 점검하세요. 삽입 여부를 정확히 구분할 수 있도록 벡터와 insert 사이 경계 부위에 프라이머를 두는 게 좋아요.
위음성(false negative)
클로닝은 잘됐는데, 밴드가 안 나오는 경우
→ 세포 파쇄 부족, PCR 조건 미세 조정, 프라이머 불안정 등이 원인이 될 수 있어요. PCR mix나 조건을 다시 체크해보세요.
콜로니 PCR을 더 잘 활용하려면?
PCR 하기 전에 콜로니 보관해두기
PCR에서 긍정 결과가 나와도, 이미 실험에 사용해버린 콜로니면 다시 찾기 어려워요.
→ PCR 하기 전, 동일한 콜로니를 LB 배지에 접종하거나 글리세롤 스톡으로 저장해두는 습관을 들이면 정말 편해요.
컨트롤 세팅은 필수!
항상 아래 세 가지는 같이 넣어주세요.
양성 대조군(positive control): 클로닝 성공한 벡터
음성 대조군(negative control): 클로닝 안 된 벡터 또는 무처리 세균
no-template control(NTC): DNA 없이 PCR mix만
콜로니 PCR은 작지만 강력한 실험이에요. 실험자의 손에 따라 성공률이 확 달라지는 민감한 기법이기도 하죠.
하지만 기본 원리만 잘 이해하고, 프라이머 설계와 세포 파쇄 조건을 꼼꼼히 조절한다면, 누구나 정확하고 빠르게 클로닝 확인을 할 수 있어요.
이제 콜로니 PCR 결과를 보고 당황하지 마세요. 차분히 조건을 확인하고, 대조군과 비교해가며 원인을 분석하면 해결 실마리가 보일 거예요!